题目内容
10.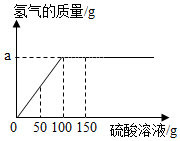 某学生为测定某铜锌合金中锌的纯度,实验方法是:取合金样品10克放入烧杯中,然后向烧杯里逐滴滴入稀硫酸溶液,到不再产生气体后,将溶液过滤,将固体洗涤烘干后,称得固体质量为3.5g,反应情况如图所示.【提示:铜不与稀硫酸溶液反应;锌与硫酸反应方程式为Zn+H2SO4=H2↑+ZnSO4】请根据图示和信息计算:
某学生为测定某铜锌合金中锌的纯度,实验方法是:取合金样品10克放入烧杯中,然后向烧杯里逐滴滴入稀硫酸溶液,到不再产生气体后,将溶液过滤,将固体洗涤烘干后,称得固体质量为3.5g,反应情况如图所示.【提示:铜不与稀硫酸溶液反应;锌与硫酸反应方程式为Zn+H2SO4=H2↑+ZnSO4】请根据图示和信息计算:(1)10克合金样品中所含铜的质量是3.5克.
(2)此铜锌合金样品中所含锌的纯度是65%.
(3)用于实验的硫酸溶液的溶质质量分数是多少?
分析 锌能与稀硫酸反应,铜不与硫酸反应,不再产生气体后剩余的固体就是铜的质量,由此可求出锌的质量即可计算出铜锌合金样品中所含锌质量分数;根据锌的质量可以求出恰好反应时硫酸中溶质的质量,再根据溶质的质量分数可求出用于实验的硫酸溶液的溶质质量分数.
解答 解:(1)由题意可知,10克合金样品中所含铜的质量是3.5克.
(2)此铜锌合金样品中所含锌的纯度是:$\frac{10g-3.5g}{10g}×100%$=65%.
(3)由生成的氢气和硫酸的关系图可知,恰好反应时硫酸溶液的质量是100g,
设100g硫酸中溶质的质量x
设稀硫酸中溶质质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 98
10g-3.5g x
$\frac{65}{98}=\frac{10g-6.5g}{x}$ 解得x=9.8g
用于实验的硫酸溶液的溶质质量分数是:$\frac{9.8g}{100g}×100%$=9.8%
故答为:(1)3.5g;(2)65%;(3)用于实验的硫酸溶液的溶质质量分数是9.8%
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图表信息,确定恰好反应时反应的硫酸的质量是计算用于实验的硫酸溶液的溶质质量分数的关键.

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
1.下列事实不能用分子的特点解释的是( )
| A. | 刮风时尘土飞扬 | |
| B. | 将25m3的石油气装入0.024m3的钢瓶中 | |
| C. | 进入花园闻到花香 | |
| D. | 将湿手放到火炉上烤时干得快 |
15.下列实验操作不符合规范要求的是( )
| A. |  加热烧杯中液体 | B. | 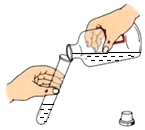 往试管中倾倒液体 | ||
| C. | 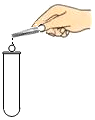 大理石放入试管 | D. | 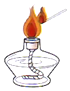 点燃酒精灯 |
19.下列有关化合价的叙述正确的是( )
| A. | 有些元素在不同条件下可表现出不同化合价 | |
| B. | 氨气(NH3)中氮元素的化合价为+3 | |
| C. | 氧气中氧元素的化合价为-2 | |
| D. | 化合价与原子最外层电子数无关 |
20.农业上常用质量分数为4%的NaCl溶液来选种,现有20%的NaCl溶液100g,如打算全部用来选种,需要另加蒸馏水( )
| A. | 200g | B. | 300g | C. | 400g | D. | 500g |


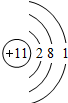 ,④一个化合反应的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
,④一个化合反应的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.