题目内容
19.下列有关化合价的叙述正确的是( )| A. | 有些元素在不同条件下可表现出不同化合价 | |
| B. | 氨气(NH3)中氮元素的化合价为+3 | |
| C. | 氧气中氧元素的化合价为-2 | |
| D. | 化合价与原子最外层电子数无关 |
分析 A、根据常见元素的化合价,进行分析判断.
B、根据在化合物中正负化合价代数和为零,结合氨气的化学式进行解答.
C、根据单质中元素的化合价为0进行分析判断.
D、化合价与原子最外层电子数有着密切的关系.
解答 解:A、有些元素在不同条件下可表现出不同化合价,如在N2(单质)中氮元素显0价,在KNO3中氮元素显+5价,故选项说法正确.
B、氢元素显+1价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(+1)×3=0,则x=-3价,故选项说法错误.
C、根据单质中元素的化合价为0,氧气属于单质,故氧元素的化合价为0,故选项说法错误.
D、元素的最高正化合价的数值等于:原子的最外层电子数目;非金属元素的负化合价的数值等于:原子的最外层电子数目-8,故选项说法错误.
故选:A.
点评 本题难度不大,掌握单质中元素的化合价为0、在化合物中正负化合价代数和为零等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
9. 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是Fe3O4.
【实验探究】取少量黑色固体于试管中,加入足量的稀盐酸,固体全部溶解,有气泡冒出,证实猜想一是正确的.产生气泡的原因用化学方程式表示Fe+2HCl═FeCl2+H2↑
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O(气)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该试管中剩余固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是Fe3O4.
【实验探究】取少量黑色固体于试管中,加入足量的稀盐酸,固体全部溶解,有气泡冒出,证实猜想一是正确的.产生气泡的原因用化学方程式表示Fe+2HCl═FeCl2+H2↑
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O(气)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该试管中剩余固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
7.实验室用下表中方法制取氧气.
请任选一种方法的数据,计算x或y(写出计算过程).
| 反应物 | 条件 | 生成O2质量 | |
| 方法1 | KMnO4固体31.6g | 加热 | x |
| 方法2 | 质量为y的KClO3固体 | 加热、少量MnO2 | 4.8g |
14. 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )| A. | HCl NaOH BaCl2 Na2SO4 | B. | HCl Ba(OH)2 Na2SO4 BaCl2 | ||
| C. | H2SO4 Ba(OH)2 Na2SO4 BaCl2 | D. | H2SO4 NaOH BaCl2 Na2SO4 |
4.自来水厂使用氯气(Cl2)对水进行消毒,氯气中氯元素的化合价为( )
| A. | -1 | B. | 0 | C. | +1 | D. | +5 |
11.单酸(H2C2O4)在一定条件发生如下反应:aH2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$bH2O↑+cCO2↑+dX↑
取18g草酸,加热至完全分解,反应后测得生成水蒸气3.6g,生成二氧化碳8.8 g.下列说法正确的是( )
取18g草酸,加热至完全分解,反应后测得生成水蒸气3.6g,生成二氧化碳8.8 g.下列说法正确的是( )
| A. | b=c | B. | a=b+c+d | ||
| C. | 气体X中含氢元素 | D. | 气体X的质量为2.8g |
8.某反应的化学方程式为:A+2B=2C+D,若6克A与22克B恰好完全反应,生成D的质量为7克,同时生成C的质量为( )
| A. | 11克 | B. | 21克 | C. | 29克 | D. | 65克 |
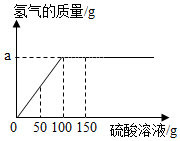 某学生为测定某铜锌合金中锌的纯度,实验方法是:取合金样品10克放入烧杯中,然后向烧杯里逐滴滴入稀硫酸溶液,到不再产生气体后,将溶液过滤,将固体洗涤烘干后,称得固体质量为3.5g,反应情况如图所示.【提示:铜不与稀硫酸溶液反应;锌与硫酸反应方程式为Zn+H2SO4=H2↑+ZnSO4】请根据图示和信息计算:
某学生为测定某铜锌合金中锌的纯度,实验方法是:取合金样品10克放入烧杯中,然后向烧杯里逐滴滴入稀硫酸溶液,到不再产生气体后,将溶液过滤,将固体洗涤烘干后,称得固体质量为3.5g,反应情况如图所示.【提示:铜不与稀硫酸溶液反应;锌与硫酸反应方程式为Zn+H2SO4=H2↑+ZnSO4】请根据图示和信息计算: