题目内容
16.下列装置图与氧气的制取和性质有关:(1)根据如图(A--D)所给的装置,回答问题

①实验室用高锰酸钾制取氧气,可选用的发上装置为A;
②实验室用过氧化氢在二氧化锰催化下产生氧气,可选用的发生装置为B;
③如果用C装置收集氧气,气体应从b口进(填a或b);
④如果用D装置收集氧气,气体应从c口进(填c或d).

(2)如图所示,在盛水的试管中放一根洁净的铁钉,用带U型管塞塞紧,U型管内水面处于同一高度,放置几天后观察到U型管内的水面A(填字母).
A、a比b高 B、b比a高 C、一样高 D、无法判断.
分析 (1)①从用加热高锰酸钾的方法制取氧气,是加热固体制取气体去分析;
②从过氧化氢溶液在二氧化锰催化作用下生成水和氧气,是固体和液体反应且不需加热去分析;
③从如果用C装置收集氧气,气体应从b进入去分析;
④从如果用D装置收集氧气,由于装置内充满水,氧气从c管进入,瓶中的水从d管中排出去分析;
(2)根据钢铁生锈的条件是钢铁与氧气和水同时接触.酸性溶液、碱性溶液、盐溶液能促进金属生锈进行分析.
解答 解:(1)①用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成;由于是加热固体制取气体,所以发生装置可应选A;
②过氧化氢溶液在二氧化锰催化作用下生成水和氧气,是固体和液体反应且不需加热,所以发生装置应选B;
③如果用C装置收集氧气,气体应从b进入,由于氧气的密度比空气大,进入集气瓶后,沉积在下面,氧气自下而上充满集气瓶,瓶中的空气从a导管中排出;
④如果用D装置收集氧气,由于装置内充满水,氧气从c管进入,瓶中的水从d管中排出;
(2)铁钉与水和氧气充分接触,容易生锈.铁钉生锈时消耗了试管中的氧气,从而使得试管内的气体压强减小,在外界大气压的作用下,使得U型管内液面a处液面上升,b处液面下降,故选:A.
故答案为:(1)①A;
②B;
③b;
④c;
(2)A.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
4.有四种物质的溶液:①NaOH ②MgSO4 ③HNO3 ④CuSO4,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是( )
| A. | ④③②① | B. | ④①②③ | C. | ①③④② | D. | ①④②③ |
11.工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3 晶体的原因是KClO3在常温下溶解度较小.
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
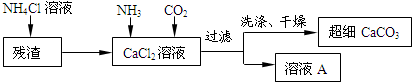
(5)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.检验CaCO3是否洗涤干净的方法是取最后一次的洗涤液加硝酸银溶液,如有沉淀生成则没有洗干净,反之以洗干净.
(6)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)为常见的两种化合物,其中碳酸钠最为重要,在工业上有广泛的应用.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(5)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.检验CaCO3是否洗涤干净的方法是取最后一次的洗涤液加硝酸银溶液,如有沉淀生成则没有洗干净,反之以洗干净.
(6)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)为常见的两种化合物,其中碳酸钠最为重要,在工业上有广泛的应用.
1.现有CO、CO2、H2、O2和N2的混合气依次通过石灰水、热的铜网、灼热的氧化铜,若每次都完全反应,冷却至室温,最后剩余的气体是( )
| A. | N2和CO | B. | O2和N2 | C. | CO2和N2 | D. | 只有N2 |
 用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧来测定氧气在空气中含量的方法.实验操作有如下主要步骤:①将燃烧匙伸入广口瓶,并塞上塞子 ②点燃燃烧匙中的红磷 ③先用弹簧夹夹紧乳胶管 ④燃烧完全并冷却后,打开弹簧夹.
用来测定空气成分的方法很多,图1所示的是小明用红磷在空气中燃烧来测定氧气在空气中含量的方法.实验操作有如下主要步骤:①将燃烧匙伸入广口瓶,并塞上塞子 ②点燃燃烧匙中的红磷 ③先用弹簧夹夹紧乳胶管 ④燃烧完全并冷却后,打开弹簧夹.