题目内容
15.有10克氧化铜、氢氧化铜、硫酸铜的混合物与100克9.8%的稀硫酸恰好完全反应,则反应后所得溶液中的溶质质量可能为( )| A. | 17克 | B. | 18克 | C. | 19克 | D. | 22克 |
分析 根据已有的知识进行,氧化铜、氢氧化铜、硫酸铜与硫酸反应生成硫酸铜,可以根据质量守恒定律,根据硫酸的质量即可求出生成硫酸铜的质量.
解答 解:假如是氧化铜和硫酸铜的混合物,则有
CuO----H2SO4--生成的CuSO4
80 98 160
8g 9.8g 16g
则原混合物中硫酸铜的质量为10g-8g=2g,则所得溶液中溶质的质量为18g.
假如是氢氧化铜和硫酸铜的混合物,则有
Cu(OH)2----H2SO4--生成的CuSO4
98 98 160
9.8g 9.8g 16g
则原混合物中硫酸铜的质量为10g-9.8g=0.2g,则所得溶液中溶质的质量为0.2g+16g=16.2g
由于是三者的混合物,则对应的溶液中的溶质的质量是大于16.2g小于18g,则答案为A.
故选A.
点评 本题主要考查了质量守恒定律方面的内容或根据化学方程式的计算,完成此题,也可以依据反应的化学方程式结合题干提供的数据进行.

练习册系列答案
相关题目
20.用定量研究的方法得出了空气是由氮气和氧气组成的科学家是( )
| A. | 侯德榜 | B. | 道尔顿 | C. | 门捷列夫 | D. | 拉瓦锡 |
1.水果具有芳香气味是因其含有乙酸乙酯(C4H8O2),关于乙酸乙酯说法正确的是( )
| A. | 乙酸乙酯是一种氧化物 | |
| B. | 乙酸乙酯由14个原子构成 | |
| C. | 乙酸乙酯分子由碳、氢、氧原子构成 | |
| D. | 乙酸乙酯含有4个碳元素、8个氢元素、2个氧元素 |
3.下列实验方法的设计,合理的是( )
| A. | 除去CO还原Fe2O3的尾气中含有的CO:用酒精灯点燃 | |
| B. | 制取NaOH固体:将适量的Na2CO3溶液与Ca(OH)2溶液混合,过滤 | |
| C. | 分离NaCl和CaCl2溶液:取样,加入Na2CO3溶液,充分反应后,过滤 | |
| D. | 证明NaOH溶液部分变质:加入过量的CaCl2溶液,再滴入酚酞溶液,观察 |
20.下列有关物质鉴别的方案,可行的是( )
①利用CO2气体能区分NaOH、Ca(OH)2和稀盐酸三种溶液;
②只用蒸馏水,就能鉴别固体烧碱和纯碱两种物质;
③不用其它任何试剂就能将HCl、BaCl2、Na2C03、NaCl四种溶液鉴别出来.
①利用CO2气体能区分NaOH、Ca(OH)2和稀盐酸三种溶液;
②只用蒸馏水,就能鉴别固体烧碱和纯碱两种物质;
③不用其它任何试剂就能将HCl、BaCl2、Na2C03、NaCl四种溶液鉴别出来.
| A. | 只有①可行 | B. | 只有②③可行 | C. | 只有①③可行 | D. | ①②③都可行 |
7.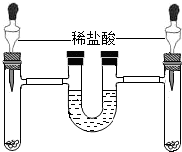 如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
 如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )| A. | 右试管中溶液为浅绿色 | |
| B. | 两试管中所得溶液的质量相等 | |
| C. | U型管中液面左升右降 | |
| D. | 右试管比左试管中产生气泡的速率快 |
4.某工厂在装配一件设备时,不小心把一个用镁合金制造的精密空心小球(已知该小球的密度为1.60g/cm3)掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来,有人提出往小洞中倒入某种溶液使小球浮起的方法.现有三种物质的溶解度数据(注:水的密度为1g/cm3,溶液的体积变化忽略不计.).在保证不损坏小球的前提下,理论上可以用上表中物质配制成溶液,倒入小洞中使小球浮起,该溶液可以选择( )
| 物质 | 溶解度/克 | ||||
| 20℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
| 硝酸铜 | 125.1 | 159.8 | 178.8 | 207.8 | 239.6 |
| 硝酸钾 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
| 氯化钾 | 34.0 | 40.0 | 45.0 | 51.1 | 56.7 |
| A. | 20℃的饱和硝酸铜溶液 | B. | 20℃的饱和硝酸钾溶液 | ||
| C. | 40℃的饱和硝酸钾溶液 | D. | 80℃的饱和氯化钾溶液 |
5.钾肥能使作物茎秆长得坚强,防止倒伏,促进开花结实,增强抗旱、抗寒、抗病虫害能力.下列属于钾肥的是( )
| A. | KCl | B. | (NH4)2SO4 | C. | CO(NH2)2 | D. | Ca3(PO4)2 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: