网址:http://m.1010jiajiao.com/timu_id_4455043[举报]
①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
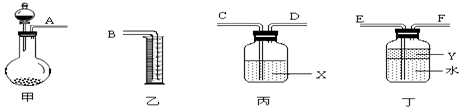
③用右图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中
(3)液体X是
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是
A.苯B.四氯化碳C.酒精D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况).
(5)对获得准确的气体体积无益的操作有
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g.根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是
按下图所示装置,用两种不同操作分别进行实验,观察B管中现象。

操作1:先夹紧止水夹a,再使A管开始反应,实验中B管观察到的现象是_______________。B管发生反应的离子方程式是____________________________________________________。
操作2:打开止水夹a,使A管开始反应一段时间后再夹紧止水夹a,实验中在B管观察到的现象是_____________________,B管中发生反应的离子方程式是?__________________。
查看习题详情和答案>>按图6-27中所示装置,用两种不同操作分别进行实验,观察B管中的现象。

图6-27
操作Ⅰ:先夹紧止水夹a,再使A管开始反应。实验中在B管中观察到的现象是_____________。B管中发生的反应的离子方程式是:___________________________。
操作2:打开止水夹a,使A管开始反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是_________________。B管中发生的反应的离子方程式是_________________。
查看习题详情和答案>>(1)按图Ⅰ中所示装置,用两种不同操作分别进行实验,观察B管中现象。
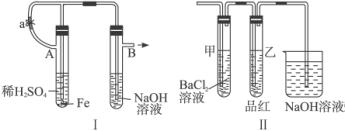
操作1:先夹紧止水夹a,再使A管开始反应,实验中在B管中观察到的现象是____________________________________________________________________。
B管中发生反应的离子方程式是______________________________________________。
操作2:打开止水夹a,使A管开始反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是________________________________________________________________。
(2)上述装置的实验结束后,取A管内反应所得溶液,隔绝空气小心蒸干后,再高温煅烧(有关装置及操作已略去),最后留下红色固体。将分解时产生的气体按图Ⅱ所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内溶液红色褪色,回答:
①用化学方程式说明试管甲产生白色沉淀的原因(不用文字说明)____________________。
②根据实验现象,写出图Ⅰ中A管内溶液蒸干后,在高温下煅烧分解时所发生的氧化还原反应的化学方程式_____________________________________________________。
这个反应的氧化剂是_______________________,还原剂是____________________________。
查看习题详情和答案>>
(1)装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气________________________________________________________。
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:________________________。

(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的容器中应加入的试剂的名称及其作用:
A中加入的试剂是_________,作用是____________________________________。
B中加入的试剂是_________,作用是____________________________________。
C中加入的试剂是_________,作用是除尽__________________气体。
D中加入的试剂是_________,作用是____________________________________。
(4)实验时,C中应观察到的现象是____________________________________。
查看习题详情和答案>>