24、(7分)(1)用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出丁烷燃烧的热化学方程式____________,已知1mol液态水气化时需要吸收44kJ的热量,则1mol丁烷完全燃烧生成二氧化碳和水蒸汽时的ΔH为____________。
 (2)化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单的理解为断开1 mol 化学键时所需吸收的能量。下表是部分化学键的键能数据:
(2)化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单的理解为断开1 mol 化学键时所需吸收的能量。下表是部分化学键的键能数据:
|
化学键 |
P-P |
P-O |
O=O |
P=O |
|
键能/ kJ·mol–1 |
197 |
360 |
499 |
X |
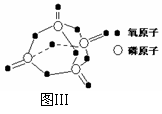
 已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中X=
。
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中X=
。
22、(12分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
① 将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2-3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
② 将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
③ 向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂恰好变色,且30秒不变化,测得所耗盐酸的体积为V1mL;
④ 重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)锥形瓶中的溶液从___________色变为___________色时,停止滴定。
 (2)滴定时边滴边摇动锥形瓶,眼睛应观察__________;
(2)滴定时边滴边摇动锥形瓶,眼睛应观察__________;
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是__________,由此造成的测定结果
___________ (填偏高、偏低或无影响);
(4)步骤②缺少的操作是________;
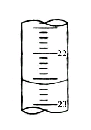
(5)右图,是某次滴定时的滴定管中的液面,其读数为__________mL;
(6)根据下列数据:
|
滴定次数[ |
待测液体积(mL)[ |
标准盐酸体积(mL) |
|
|
滴定前读数(mL) |
滴定后读数(mL) |
||
|
第一次 |
25.00 |
0.50 |
20.40 |
|
第二次 |
25.00 |
4.00 |
24.10 |
请计算待测烧碱溶液的浓度为__________ mol/L
 N2O4(g);△H<0。现将一定量NO2和N2O4的
N2O4(g);△H<0。现将一定量NO2和N2O4的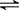 2C(g) DH<0
2C(g) DH<0
 (1)若起始温度相同,分别向三个容器中充入3molA和1molB,则达到平衡时各容器中C物质的百分含量由大到小的顺序为(填容器编号)
。
(2)若维持温度不变,起始时②中投入3molA、1molB;③中投入6molA、2molB,则达到平衡时,两容器中B的转化率② ③(填<、>或=)。
(1)若起始温度相同,分别向三个容器中充入3molA和1molB,则达到平衡时各容器中C物质的百分含量由大到小的顺序为(填容器编号)
。
(2)若维持温度不变,起始时②中投入3molA、1molB;③中投入6molA、2molB,则达到平衡时,两容器中B的转化率② ③(填<、>或=)。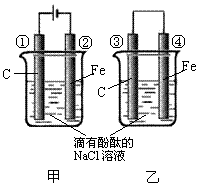 (9分)化学能和电能的相互转化,是能量转化的重要方式之一,右图两个实验装置是实现化学能和电能相互转化的装置。
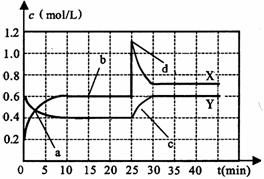
(9分)化学能和电能的相互转化,是能量转化的重要方式之一,右图两个实验装置是实现化学能和电能相互转化的装置。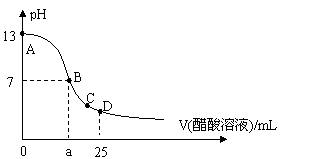 在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系正确的是
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如下图所示,有关粒子浓度关系正确的是