16、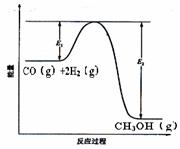 甲醇(CH3OH)是一种重要的化工原料,合成甲醇的主要反应为:CO(g)+2H2(g)
甲醇(CH3OH)是一种重要的化工原料,合成甲醇的主要反应为:CO(g)+2H2(g) CH3OH(g)
反应过程中的能量变化如图所示。
CH3OH(g)
反应过程中的能量变化如图所示。
(1)CO(g)+2H2(g) CH3OH(g)ΔH 0(填<、=、>)
CH3OH(g)ΔH 0(填<、=、>)
(2)反应体系中加入催化剂对反应热是否有影响?____ _____,原因是____ __:
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
(4)在一定条件下,上述反应在一密闭容器中达到平衡。在保证H2浓度不变的情况下,增大容器的体积,平衡____________(填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的理由是__________________________________________________。
(5)原料气的加工过程中常常混有一定量CO2,为了研究不同温度下CO2对该反应的影响,以CO2、CO和H2的混合气体为原料在一定条件下进行实验,结果表明,原料气各组分含量不同时,反应生成甲醇和副产物甲烷的碳转化率是不相同的。实验数据见下表:
|
CO2%-CO%-H2% (体积分数) |
0–30–70 |
2–28–70 |
4–26–70 |
8–22–70 |
20–10–70 |
|||||||||||
|
反应温度/℃ |
225 |
235 |
250 |
225 |
235 |
250 |
225 |
235 |
250 |
225 |
235 |
250 |
225 |
235 |
250 |
|
|
碳转化率(%) |
CH3OH |
4.9 |
8.8 |
11.0 |
36.5 |
50.7 |
68.3 |
19.0 |
33.1 |
56.5 |
17.7 |
33.4 |
54.4 |
8.0 |
12.0 |
22.6 |
|
CH4 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
2.8 |
2.8 |
2.8 |
由上表数据可得出多个结论。
结论一:在一定条件下,反应温度越高,碳转化率 ;
结论二:__________________________________________________________。
答案2009.11
总分:
 第一部分 选择题 (共36分)
第一部分 选择题 (共36分)
14、某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究规格(粗、细)对大理石该反应速率的影响;) |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
 某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。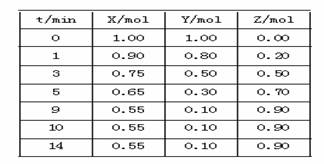
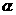 等于
_。
等于
_。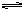 N2O4(气)△H<0,
N2O4(气)△H<0,  反应:L(固)+aG(气)
反应:L(固)+aG(气) bR(气)达到平衡时,温度和压强对该反应的影响图所示:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
( )
bR(气)达到平衡时,温度和压强对该反应的影响图所示:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
( )