12.(6分)镁是重要的金属材料,广泛应用于合金、火箭和飞机制造业,世界上大部分镁是从海水中提取的。威海是一座滨海城市,海岸线长达1000 km,海水资源丰富。某校学习小组的同学对家乡附近海水中镁元素的含量进行测定。称取海水100kg,然后再加入足量的氢氧化钠溶液,过滤、干燥、称量后得到沉淀质量见下表。(重复实验三次)。
|
|
第一次实验 |
第二次实验 |
第三次实验 |
|
所取海水质量/kg |
100 |
100 |
100 |
|
生成沉淀质量/kg |
0.28 |
0.29 |
0.30 |
试计算海水中镁元素的质量分数。
(假定海水中镁元素全部以氯化镁的形式存在,不考虑沉淀中杂质的干扰)。
10.(4分)下表是不同溶质质量分数的硫酸溶液和氨水与其相应密度的对照表
|
溶液中溶质的质量分数 |
4% |
2% |
16% |
24% |
28 |
|
硫酸溶液的密度(20℃)/g·ml |
1.02 |
1.08 |
1.11 |
1.17 |
1.20 |
|
氨水的密度(20~C)/g·ml |
0.98 |
0.95 |
0.94 |
0.91 |
0.90 |
请你仔细分析上表中的数据,回答下列问题:
(1)从上表可以看出,硫酸溶液的密度大于水的密度,而氨水的密度则小于水的密
度。除此以外,你还能够总结出溶液密度与其溶质的质量分数的变化规律是
。
(2)试从物质定量组成(氨水的溶质为NH3)的角度分析,为什么这两种溶液密度与其溶质的质量分数之间存在这种变化规律?
。

 日常生活中,我们经常饮用矿泉水。右图是某饮用天然水部分商标图,图中列出了理化指标。据此回答2-3题
日常生活中,我们经常饮用矿泉水。右图是某饮用天然水部分商标图,图中列出了理化指标。据此回答2-3题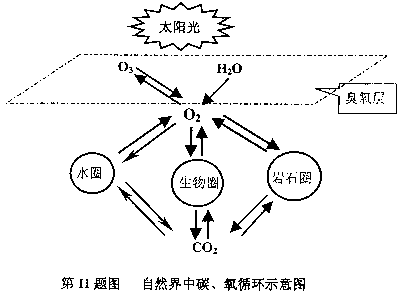 下图是自然界中碳、氧循环的主要途径:
下图是自然界中碳、氧循环的主要途径: (4)另外有一种实验室产生少量氧气的简易方法:用过氧化氢的水溶液做反应物,反应条件是常温和二氧化锰做催化剂,反应的化学方程式为
。
(4)另外有一种实验室产生少量氧气的简易方法:用过氧化氢的水溶液做反应物,反应条件是常温和二氧化锰做催化剂,反应的化学方程式为
。 (8分)人类对原子结构的认识是逐渐深入的。右图是不同时期科学家提出的原子结构模型。
(8分)人类对原子结构的认识是逐渐深入的。右图是不同时期科学家提出的原子结构模型。 
