0 22464 22472 22478 22482 22488 22490 22494 22500 22502 22508 22514 22518 22520 22524 22530 22532 22538 22542 22544 22548 22550 22554 22556 22558 22559 22560 22562 22563 22564 22566 22568 22572 22574 22578 22580 22584 22590 22592 22598 22602 22604 22608 22614 22620 22622 22628 22632 22634 22640 22644 22650 22658 447348
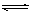 HCO3�C+OH�C,�� HCO3�C+ H2O
HCO3�C+OH�C,�� HCO3�C+ H2O