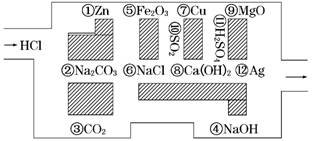
22.(11分)(2010·临沂模拟)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH、Mg2+、CO、Ba2+、SO.将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
|
实验 序号 |
实验内容 |
实验结果 |
|
1 |
加AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12 L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27 g,第二次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是____________(填“一定存在”“一定不存在”或“不能确定”);根据实验1-3判断混合物中一定不存在的离子是________.
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
|
阴离子符号 |
物质的量浓度(mol/L) |
|
|
|
|
|
|
|
|
|
(3)试确定K+是否存在?________,判断的理由是________________________________
______________________________________________________________.
解析:该混合物溶于水后得澄清溶液,说明Ba2和SO不能同时存在,加足量NaOH溶液并加热产生气体,说明存在NH,由1.12 L氨气可知,NH的物质的量为0.05 mol,在第三步操作中,沉淀有两种,说明存在SO和CO,则该混合物中不存在Ba2+,同时也不存在Mg2+.由沉淀的质量求出SO的物质的量为0.01 mol,CO的物质的量为0.02 mol,加AgNO3溶液有沉淀,并不能确定有Cl-,因为Ag+与SO和CO都能产生沉淀.根据离子所带的正、负电荷数相等可知,K+一定存在,但是K+的物质的量不能确定,因为Cl-是否存在并不明确.
答案:(1)不能确定 Ba2+、Mg2+
(2)
|
阴离子符号 |
物质的量浓度(mol/L) |
|
SO |
0.1 |
|
CO |
0.2 |
(3)存在 溶液中肯定存在的离子是NH、CO和SO.经计算,NH的物质的量为0.05 mol,CO、SO的物质的量分别为0.02 mol和0.01 mol,根据电荷守恒,得K+一定存在。
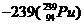 ,这种
,这种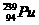 可由铀
可由铀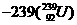 经过多次β衰变而得,下列有关
经过多次β衰变而得,下列有关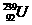 的说法中正确的是
的说法中正确的是 (3)
(3) 
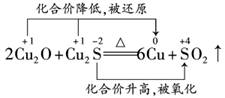
 (1)请用上述物质填空,并配平化学方程式:
(1)请用上述物质填空,并配平化学方程式: