0 19742 19750 19756 19760 19766 19768 19772 19778 19780 19786 19792 19796 19798 19802 19808 19810 19816 19820 19822 19826 19828 19832 19834 19836 19837 19838 19840 19841 19842 19844 19846 19850 19852 19856 19858 19862 19868 19870 19876 19880 19882 19886 19892 19898 19900 19906 19910 19912 19918 19922 19928 19936 447348
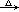 C2H5Br+H2O
C2H5Br+H2O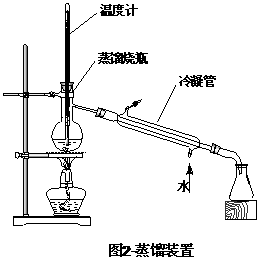
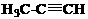 ②C3H8
③CH3-C≡C-CH2-CH3
②C3H8
③CH3-C≡C-CH2-CH3 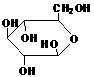 ⑤
⑤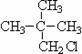 ⑥
⑥ 
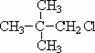 ⑧
⑧ ⑨
⑨

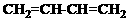
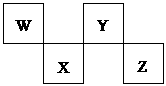 (共9分)W、X、Y、Z 4种短周期元素在元素周期表中位置如图所示,其中Z位于ⅥA族。请回答下列问题。
(共9分)W、X、Y、Z 4种短周期元素在元素周期表中位置如图所示,其中Z位于ⅥA族。请回答下列问题。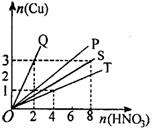 (共3分)铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应:
(共3分)铜和硝酸反应的物质的量的关系如图所示,纵坐标表示消耗铜的物质的量,横坐标表示消耗硝酸的物质的量,坐标图中各条线表示下列反应: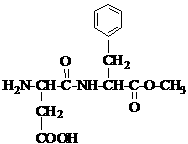 2009年6月,委内瑞拉卫生部宣布,停止在该国市场上销售“零度”可口可乐,原因是这种可乐含有对人体有害的成分。其中,因使用甜味剂阿斯巴甜(ASPARTAME)一度引发人们的质疑。阿斯巴甜是一种常见的食品添加剂。然而随着近年英国、意大利等地出现了阿斯巴甜的致癌说,这种添加剂开始备受争议。其结构简式如右图所示。下列关于阿斯巴甜的说法不正确的是( )
2009年6月,委内瑞拉卫生部宣布,停止在该国市场上销售“零度”可口可乐,原因是这种可乐含有对人体有害的成分。其中,因使用甜味剂阿斯巴甜(ASPARTAME)一度引发人们的质疑。阿斯巴甜是一种常见的食品添加剂。然而随着近年英国、意大利等地出现了阿斯巴甜的致癌说,这种添加剂开始备受争议。其结构简式如右图所示。下列关于阿斯巴甜的说法不正确的是( )