18.(8分)下表是生活生产中常见的物质,表中列出了它们的一种主要成分 (其它成分未列出)
|
编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
|
名称 |
绿矾 |
醋精 |
苏打 |
酒精 |
铜导线 |
蔗糖 |
烧碱 |
|
主要成分 |
FeSO4 |
CH3COOH |
Na2CO3 |
CH3CH2OH |
Cu |
C12H12O11 |
NaOH |
(1)请你对表中①-⑦的主要成分进行分类(填编号)
属于盐的是 属于电解质的是 属于非电解质的是
(2)写出②与⑦反应的化学方程式
过量盐酸与③反应的离子方程式

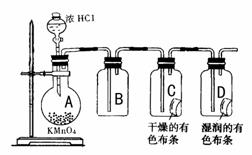 (12分)某学习小组通过上网查阅资料得知:实验室可以用KMnO4与浓盐酸在常温下反应制取氯气,其反应的化学方程式为2KMnO4+16HCI(浓)=2KCI+2MnCl2+5Cl2↑+8H2O ,据此,他们设计了以下实验方案探究Cl2的性质。
(12分)某学习小组通过上网查阅资料得知:实验室可以用KMnO4与浓盐酸在常温下反应制取氯气,其反应的化学方程式为2KMnO4+16HCI(浓)=2KCI+2MnCl2+5Cl2↑+8H2O ,据此,他们设计了以下实验方案探究Cl2的性质。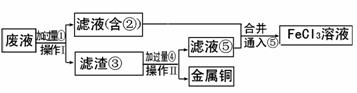
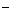 +HC1O
+HC1O