27.(15分)剪秋箩是雌雄异株(XY型性别决定)的二倍体高等植物,繁殖能力强,后代数量多。其叶形有宽叶、窄叶两种类型(受一对等位基因控制),且有配子致死现象。某科学家在研究剪秋箩叶形性状遗传时,做了如下杂交实验:
|
杂交(组) |
亲代 |
子代 |
||
|
雌 |
雄 |
雌 |
雄 |
|
|
1 |
宽叶 |
窄叶 |
无 |
全部宽叶 |
|
2 |
宽叶 |
窄叶 |
无 |
1/2宽叶、1/2窄叶 |
|
3 |
宽叶 |
宽叶 |
全部宽叶 |
1/2宽叶、1/2窄叶 |
(1)根据上述实验结果,可判断剪秋箩窄叶是由 染色体上的 性基因控制。
(2)第1、2组后代没有雌性个体,最可能的原因是 。为进一步证明上述结论,某课题组同学决定对剪秋箩自然种群进行调查。如果在自然种群中不存在 (写表现型)剪秋箩,则上述假设成立。
(3)让第3组子代中的宽叶雌、雄个体进行杂交,其后代中宽叶与窄叶的比例为 。
(4)剪秋萝的花色中红花对白花是显性,且无配子致死现象。现用一株双杂合的宽叶红花雌株与窄叶白花雄株杂交,若子代表现型及比例为 时,则说明控制剪秋萝叶形和花色的两对基因位于 染色体上,它们的遗传符合基因自由组合定律。
[选考部分](共35分)
第Ⅱ卷选考部分共5题,共35分。其中第28、29题为物理题,第30、31题为化学题。考生从两道物理、两道化学题中各任选一题作答,若28、29题都作答,则按第28题计分,若第30、31题都作答,则按第30题计分;第32题为生物题,是必答题。请将答案都填写在答题卡选答区域的指定位置上。
26. (25分)回答下列Ⅰ、Ⅱ题
(25分)回答下列Ⅰ、Ⅱ题
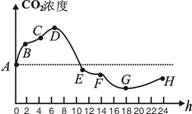
Ⅰ.(15分)下图是某地农民蔬菜大棚内夏季晴天一
昼夜CO2浓度的变化情况,分析并回答下列问题:
(1)图中D点表示大棚内生物呼吸作用释放的二
氧化碳量等于 。
(2)据图分析,蔬菜在24小时内 (能、不
能)积累有机物。大棚内每天要适当通风,以补充 ,否则蔬菜将不能生长。
(3)已知在自然情况下,温度在20℃-40℃时,光饱和点(当达到一定光照强度时,光合速率不再增加,此时的光照强度为光饱和点)均在30000 Lx以上。现已测得大棚内E点时光照强度为8000Lx,温度为25℃,F点时光照强度为20000Lx,温度为38℃。欲证明图中EF段较DE段CO2浓度降低减缓,主要是受温度而不是受光照强度的影响,有人利用下面装置予以验证,请将实验处理补充完整。
组 别K^S*5U.C#O |
1 |
2 |
3 |
4 |
光照强度(Lx) |
8000 |
① |
20000 |
8000 |
温度(℃) |
25 |
38 |
② |
③ |
实验1小时后,测定四组装置内CO2浓度,若分别为a、b、c、d,且它们之间数量关系为 (用字母和“≈、<、>”表示),则说明影响EF段CO2浓度降低减缓的主要原因是温度而不是光照强度
Ⅱ.(10分)下图表示人体内生命活动调节系统的部分结构和关系的示意图,请据图回答:
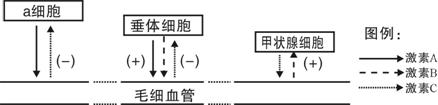
(1)激素B是 ,其分泌量的多少受 和 (写名称)两种信息分子的调节。
(2)人在突遇寒冷刺激的情况下,激素C的分泌量会迅速增多。此时激素C的分泌活动主要受 调节,此过程中甲状腺是 (结构)
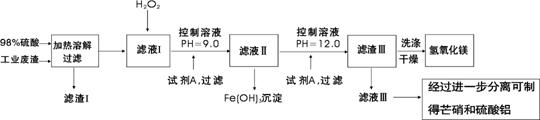
24.(15分)某工厂废渣含MgCO3、SiO2、Fe2O3 、FeCO3和CaCO 3 、Al2O3 。科研小组拟对废渣进行综合利用制取氢氧化镁、芒硝(Na2SO4·10H2O)和硫酸铝,设计如下工艺:
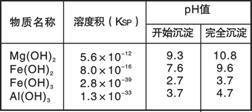 右表为几种沉淀的相关数据。回答以下问题:
右表为几种沉淀的相关数据。回答以下问题:
(1)滤渣Ⅰ中主要成分是CaSO4和
(填化学式)。
(2)欲检验滤液Ⅰ中是否含有Ca2+,
能否用碳酸钠溶液? (填“行”或“不行”)。
(3)滤液Ⅰ中加入试剂后,pH必须控制为9.0。如果pH过大,可能引起的后果是 。
(4)用化学方程式表示往滤液I中加入H2O2的目的
(5)滤液Ⅱ中c(Fe3+)= 。
(6)滤液Ⅲ的主要阳离子是____________(填离子符号);欲从滤液Ⅲ中分离出硫酸铝溶液,依次加入的试剂可以是
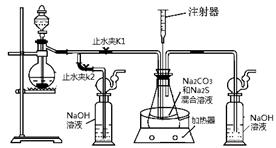
|
(1)实验时,打开K1,关闭K2,最
后洗气瓶中发生反应的离子方程式
是 。
(2)锥形瓶内溶液pH小于7时会导
致产品分解,因此实验过程中需要控制
锥形瓶内溶液的pH。
①反应过程中,锥形瓶中溶液pH将________(填“增大”、“减小”或“保持不变”)。
②测量锥形瓶中溶液pH时,用注射器吸取溶液样品比直接打开锥形瓶瓶塞取样,除操作简便外,还具有的优点是 。
③若实验过程中测得溶液pH已接近于7。此时应该进行的操作是 。
(3)已知:2Na2 S2O3 +I2=2NaI+ Na2 S4O6。实验结束后进行相关处理,可得Na2S2O3 ·5H2O
晶体。为测量其纯度,取晶体样品mg,加水溶解后,滴入几滴淀粉溶液,用0.010mol/L碘水滴定到终点时,消耗碘水溶液vmL,则该样品纯度是 。
(4)制取硫代硫酸钠的另一种方法是直接将硫粉和亚硫酸钠、水混合共热制取。为探究制取硫代硫酸钠最佳条件(如溶液pH、亚硫酸钠浓度、反应温度、硫粉质量等),设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
|
实验序号 |
溶液pH |
亚硫酸钠与水的质量比 |
反应温度 |
硫粉质量 |
亚硫酸钠转化率 |
|
1 |
10 |
1.5:1 |
100 |
18 |
80.7% |
|
2 |
a |
1.1:1 |
100 |
18 |
94.6% |
①实验1、2的目的是探究亚硫酸钠浓度对亚硫酸钠转化率的影响,则a=
②若还要探究溶液pH、反应温度、硫粉质量对亚硫酸钠转化率的影响,除实验1、2外,至少还需进行
次对比实验
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响。为什么?答:_______________。
23.(13分)以焦炭为原料的制氨流程示意如下:

I、“精制”过程是将含有少量CO、CO2、O2和H2S等杂质的原料气体通入含有氨水的醋酸亚铜二氨(化学式为[Cu (NH3)2]Ac)溶液,以获得纯净原料气。其中,吸收CO的反应为:
 CO+ [Cu (NH3)2]Ac+NH3·H2O [Cu (NH3)3CO]Ac
+H2O
CO+ [Cu (NH3)2]Ac+NH3·H2O [Cu (NH3)3CO]Ac
+H2O  <0
<0
(1)为提高CO吸收率,可采取的一项措施是_________________________。
(2)除去氧气时,氧气将 [Cu (NH3)2]Ac氧化为 [Cu (NH3)4]Ac2,则反应中还原剂与氧化剂的物质的量之比是
II、“造气”过程中。其中,焦炭与水蒸气在反应体系中将发生如下四个反应:
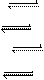 C(s)+2H2O(g) CO2(g)+2H2(g)
C(s)+2H2O(g) CO2(g)+2H2(g)  1=+90.2kJ·mol-1
1=+90.2kJ·mol-1
C(s)+H2O(g) CO(g)+ H2(g)
 2=+131.4kJ·mol-1
2=+131.4kJ·mol-1
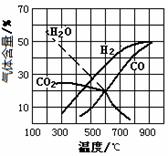 CO(g)+ H2O(g) CO2(g)+ H2(g)
CO(g)+ H2O(g) CO2(g)+ H2(g)  3
3
C(s)+ 2H2(g) CH4(g)  4
4
该体系中,一些物质的平衡组成与温度的关系图如右所示。
(3)由图可知,若采用焦炭与水蒸气反应来获得优质的水
煤气,工业生产中应尽量使焦炭和水蒸气在________(填“高
温”、“低温”或“常温”)条件下进行
(4) 3=__________________________。
3=__________________________。
(5)下表为碳与氢气合成甲烷的相关数据:
|
温度(℃) |
600 |
800 |
1000 |
|
平衡常数 |
3.2×100-146 |
1.0×10-2070 |
1.0×10-20000 |
① 4_______0(填“>”、“<”或“=”)。
4_______0(填“>”、“<”或“=”)。
②预测1000℃,焦炭与水蒸气反应体系中甲烷的含量_________
A. 几乎为0 B. 与CO浓度相当 C. 无法确定
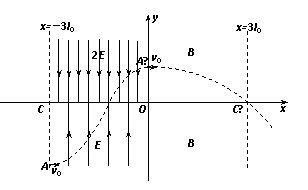 (20分)如图所示的xOy平面中,在直线x=-3l0到y轴区域内存在着两个方向相反的有界匀强电场,其中x轴上方的电场方向沿y轴负方向,x轴下方的电场方向沿y轴正方向, x轴上方的场强大小是下方的2倍, y轴右方有垂直于xOy平面的匀强磁场。在电场左边界上点A(-3l0,-2l0)处有一质量为m、电量为q带正电的微粒,以速度v0沿x轴正方向射入电场,其轨迹从y轴上的A′(0,l0)沿x轴正方向射出电场并进入磁场,并通过x轴上的点C′(3l0,0)。不计微粒的重力。K^S*5U.C#O
(20分)如图所示的xOy平面中,在直线x=-3l0到y轴区域内存在着两个方向相反的有界匀强电场,其中x轴上方的电场方向沿y轴负方向,x轴下方的电场方向沿y轴正方向, x轴上方的场强大小是下方的2倍, y轴右方有垂直于xOy平面的匀强磁场。在电场左边界上点A(-3l0,-2l0)处有一质量为m、电量为q带正电的微粒,以速度v0沿x轴正方向射入电场,其轨迹从y轴上的A′(0,l0)沿x轴正方向射出电场并进入磁场,并通过x轴上的点C′(3l0,0)。不计微粒的重力。K^S*5U.C#O (19分)如图所示,ace和bdf是间距为l的两根足够长平行导轨,其中ac、bd段光滑,ce、df段粗糙,导轨平面与水平面的夹角为θ.整个装置处在磁感应强度为B,方向垂直于导轨平面向上的匀强磁场中,ab两端连有阻值为R的电阻。若将一质量为M的金属棒置于ef端,今用大小为F,方向沿斜面向上的恒力把金属棒从ef位置由静止推至距ef端s处的cd位置(此时金属棒已经做匀速运动),现撤去恒力F,金属棒最后又回到ef端(此时金属棒也已经做匀速运动)。若不计导轨和金属棒的电阻,且金属棒与ce、df段的动摩擦因数为μ。求:
(19分)如图所示,ace和bdf是间距为l的两根足够长平行导轨,其中ac、bd段光滑,ce、df段粗糙,导轨平面与水平面的夹角为θ.整个装置处在磁感应强度为B,方向垂直于导轨平面向上的匀强磁场中,ab两端连有阻值为R的电阻。若将一质量为M的金属棒置于ef端,今用大小为F,方向沿斜面向上的恒力把金属棒从ef位置由静止推至距ef端s处的cd位置(此时金属棒已经做匀速运动),现撤去恒力F,金属棒最后又回到ef端(此时金属棒也已经做匀速运动)。若不计导轨和金属棒的电阻,且金属棒与ce、df段的动摩擦因数为μ。求: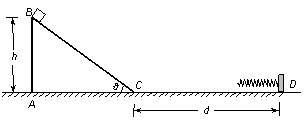 (2)小物块从开始运动到最终停止的整个过程中在斜面上运动的路程s。
(2)小物块从开始运动到最终停止的整个过程中在斜面上运动的路程s。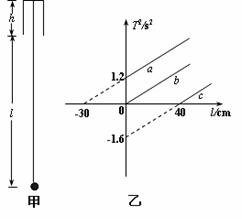 (18分)(1) 在“用单摆测定重力加速度”的实验中,将一单摆装置竖直悬于某一深度为h(未知)且开口向下的固定小筒中(单摆的下部分露于筒外),如图甲所示。将悬线拉离平衡位置一个小角度后由静止释放,设单摆摆动过程中悬线不会碰到筒壁。如果本实验的长度测量工具只能测出筒下端口到摆球球心之间的距离l。通过改变l 而测出对应的摆动周期T,作出T2 - l 图象,利用图象处理有关实验数据。
(18分)(1) 在“用单摆测定重力加速度”的实验中,将一单摆装置竖直悬于某一深度为h(未知)且开口向下的固定小筒中(单摆的下部分露于筒外),如图甲所示。将悬线拉离平衡位置一个小角度后由静止释放,设单摆摆动过程中悬线不会碰到筒壁。如果本实验的长度测量工具只能测出筒下端口到摆球球心之间的距离l。通过改变l 而测出对应的摆动周期T,作出T2 - l 图象,利用图象处理有关实验数据。 ①若欲较精确地测出电源的电动势和内阻,需扩大电压表量程,实验室中有以下四种阻值的定值电阻供选择,则定值电阻R应选取:
①若欲较精确地测出电源的电动势和内阻,需扩大电压表量程,实验室中有以下四种阻值的定值电阻供选择,则定值电阻R应选取: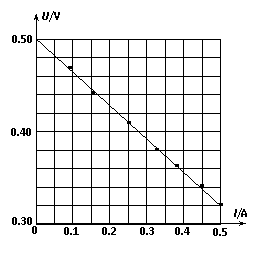 B.4000Ω
B.4000Ω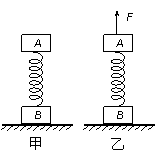 质量相等的两木块A、B用一轻弹簧栓接,静置于水平地面上,如图甲所示。现用一竖直向上的力F拉动木块A,使木块A向上做匀加速直线运动,如图乙所示。在木块A开始运动到木块B将要离开地面的过程中,弹簧始终处于弹性限度内,下述判断正确的是
质量相等的两木块A、B用一轻弹簧栓接,静置于水平地面上,如图甲所示。现用一竖直向上的力F拉动木块A,使木块A向上做匀加速直线运动,如图乙所示。在木块A开始运动到木块B将要离开地面的过程中,弹簧始终处于弹性限度内,下述判断正确的是