0 123542 123550 123556 123560 123566 123568 123572 123578 123580 123586 123592 123596 123598 123602 123608 123610 123616 123620 123622 123626 123628 123632 123634 123636 123637 123638 123640 123641 123642 123644 123646 123650 123652 123656 123658 123662 123668 123670 123676 123680 123682 123686 123692 123698 123700 123706 123710 123712 123718 123722 123728 123736 447348
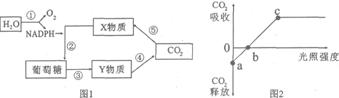
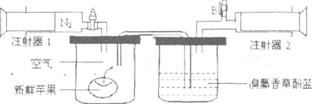
 请完成下列问题:
请完成下列问题: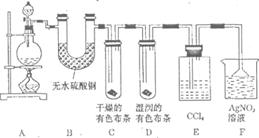
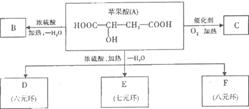
 2SO3(g);△H<0。
2SO3(g);△H<0。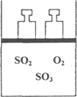
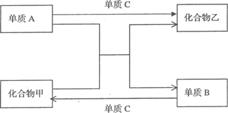
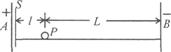
 为多少?小球自静止开始从P点运动到挡板S时,电势能是增加还是减少?改变的电势能△ε为多少?高☆考♂资♀源?网 ☆
为多少?小球自静止开始从P点运动到挡板S时,电势能是增加还是减少?改变的电势能△ε为多少?高☆考♂资♀源?网 ☆