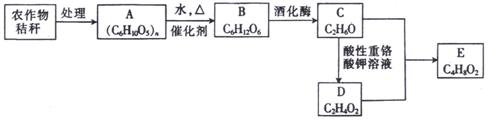
30.(12分)某试验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。
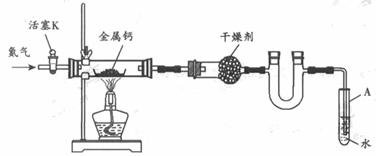
(1)按图连接好实验装置。检查装置的气密性,方法是 。
(2)反应过程中末端导管必须插入试管A的水中,目的是 (从下面选项中选填)。
A.防止倒吸;
B.防止空气中的氧气通过末端导管进入实验装置,氧化单质钙,生成氧化钙,引入杂质; C.防止尾气污染空气;
(3)制备氮化钙的操作步骤是四步:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后, ;④拆除装置,取出产物。(补充未写完整的操作)
(4)数据记录如下:
|
空瓷管质量m0/g |
瓷管与钙的质量m1/g |
瓷管与产物的质量m2/g |
|
14.80 |
15.08 |
15.15 |
①计算得到实验式CaxN2,其中x= .
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据: 。
29.(18分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,按要求回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。(用元素符号)
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________。(用化学式)
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
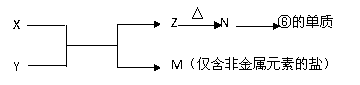
|
X溶液与Y溶液反应的离子方程式为_____________________,
N→⑥的单质的化学方程式为________________。
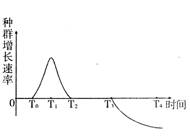 右图表示某养鱼专业户鱼塘中所养某种鱼的数量随
右图表示某养鱼专业户鱼塘中所养某种鱼的数量随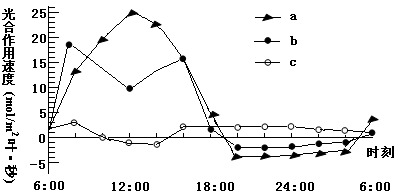

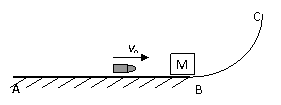 (21分) 如图所示,水平轨道AB与半径为R=360m的光滑圆弧形轨道BC相切于B点,质量为M=0.99kg的木块静止于B点,质量为m=10g的子弹以v0=500m/s的水平速度射入木块而末穿出,若木块与水平轨道间的动摩擦因数为μ=0.5,取g=10m/s2,且已知cos5°=0.966.求:子弹射入后,木块再经过多少时间方可静止?
(21分) 如图所示,水平轨道AB与半径为R=360m的光滑圆弧形轨道BC相切于B点,质量为M=0.99kg的木块静止于B点,质量为m=10g的子弹以v0=500m/s的水平速度射入木块而末穿出,若木块与水平轨道间的动摩擦因数为μ=0.5,取g=10m/s2,且已知cos5°=0.966.求:子弹射入后,木块再经过多少时间方可静止?