32.化学选考题:
A.(化学与生活)分析下面两个案例并回答有关问题。
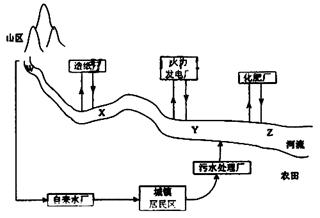 (1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
|
地点 项目 |
W |
X |
Y |
Z |
|
水温/℃ |
15 |
18 |
26 |
25 |
|
pH |
6 |
8 |
5 |
5 |
|
溶解氧量/(mg·L-1) |
11 |
9 |
7 |
3 |
①导致X、Y处水样pH变化的原因可能是 ;
②Z处鱼类大量减少,产生这种现象的原因可能是 。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O2,还含有SiO2等杂质)、煤 矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
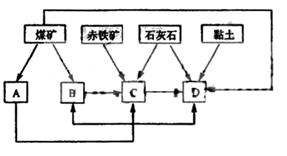
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A 、B 、C 、D ;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式 ;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可) 。
B.(物质结构)
元素A-D是元素周期表中短周期的四种元素,请根据表中的信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
物质或结构信息 |
单质制成的的高压灯,发出的黄光透雾力强、射程远。 |
工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构 |
单质常温、常压下是气体,原子的L层有一个未成对的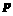 电子 电子 |
+2价阳离子的核外电子排布与氖原子相同。 |
(1)上表中与A属于同一周期的元素是_____________(写元素符号)(2分),写出D离子的电子排布式______________________。(2分)
(2)D和C形成的化合物属于_________晶体(2分)。写出C单质与水反应的化学方程式_________________________(3分)。
(3)对元素B的单质或化合物描述正确的是_________。(2分)
a.B元素的最高正价为+6 b.常温、常压下单质难溶于水
c.单质分子中含有18个电子 d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)_____。(2分)写出能证明该结论的一个实验事实________________。(2分)
C.(有机化学)
A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=CHR'在酸性高锰酸钾溶液中反应生成RCOOH和R'COOH,其中R和R'为烷基)。
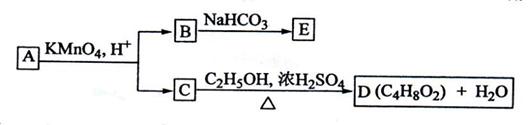
回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为_____________;(2分)B的结构简式是__________________(2分)
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1:2,则在浓硫酸的催化下,B与足量的C2H5OH发生反应的化学方程式是___________,(3分)反应类型为_____:(2分)
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是__________________(2分)
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有__________种,(2分)其相应的结构简式是__________________。(2分)
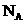 为阿佛加德罗常数,下列说法正确的是( )
为阿佛加德罗常数,下列说法正确的是( )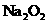 与过量的
与过量的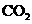 充分反应,转移电子数为
充分反应,转移电子数为 气体溶于水,溶液中
气体溶于水,溶液中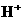 数约为
数约为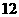 克金刚石中含共价键数目为
克金刚石中含共价键数目为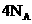

 与
与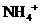 所含电子数均为
所含电子数均为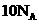
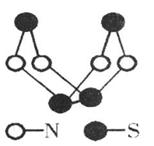 A.该物质的分子式为SN
A.该物质的分子式为SN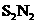 互为同素异形体
互为同素异形体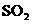 、
、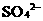 的形式被其吸收
的形式被其吸收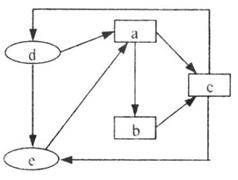 D.用无氮培养基能够直接筛选出根瘤菌
D.用无氮培养基能够直接筛选出根瘤菌 含量较低的最可能原因是分裂期细胞中的染色体高度螺旋化,不能解旋并转录成
含量较低的最可能原因是分裂期细胞中的染色体高度螺旋化,不能解旋并转录成 (2)(9分)如图8所示,己知平行玻璃砖的折射率
(2)(9分)如图8所示,己知平行玻璃砖的折射率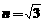 ,厚度为
,厚度为 .入射光线
.入射光线 以入射角
以入射角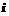 =60°射到
=60°射到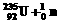 ®
® ②
②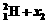 ®
®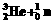
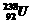 ®
®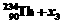 ④
④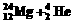 ®
®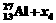
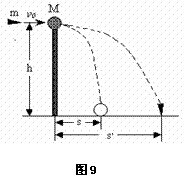 以下判断中正确的是( )
以下判断中正确的是( )