29.现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示。请根据有关信息计算:
|
硫酸配制20%的稀硫酸,以清洗钢铁表面的铁锈。他在配制
该溶液时所用98%的浓硫酸与水的质量比应该为 ▲ 。
⑵某固体物质由氯化钠和氯化钡混合组成,取32.8g该固体混
 合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如下图所示关系,计算32.8g固体混合物中氯化钡和氯化钠的质量。
合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如下图所示关系,计算32.8g固体混合物中氯化钡和氯化钠的质量。
⑶若加入的稀硫酸刚好使沉淀最大量时,将所得混合物
过滤、洗涤,得滤液200g(过程中损耗忽略不计),
计算该滤液中溶质HCl的质量分数。(若溶液中含有多种
溶质,则某溶质的质量分数为该溶质的质量与溶液总
质量之比)
(反应的方程是为:BaCl2 + H2SO4 = BaSO4↓ + 2HCl)
(注:⑵、⑶两问将计算过程写在答卷纸上)
我很自信:我已认真检查过自己的答题,一定会取得理想的成绩!
28.(10分)小杰和小燕学习了碳单质的化学性质后,知道碳与氧气反应,若反应物的量不同,生成物不同。于是两人联想到木炭粉与氧化铜发生的反应可能有:
①C+2CuO 2Cu+CO2↑
②C+CuO
2Cu+CO2↑
②C+CuO Cu+CO↑
Cu+CO↑
他们想来验证自己的想法,请你和他们一起进行探究:(请完成下列空白处)
[提出问题]木碳与氧化铜反应除生成单质铜外,另一种生成物是什么?
[猜想与假设]木炭粉与氧化铜反应生成物有三种可能:
⑴产物是铜和一氧化碳 ⑵产物是铜和二氧化碳 ⑶产物是 ①▲ 。
[设计方案]
⑴检验CO2的方法是 ②▲ 。(用方程式表示)
⑵如何检验产物中是否存在CO,两位同学分别提出了检验CO的方案,但都被大家否定了。请在下表中写出不可行的原因。
|
|
检验方案 |
不可行的原因 |
|
小杰 |
把小动物放在收集的气体中,观察能否存活 |
③▲ |
|
小燕 |
点燃生成的气体,观察能否燃烧 |
④▲ |
查阅资料后,他们把滤纸浸泡在磷钼酸与氯化钯的黄色混合液中,制成试纸(试纸遇一氧化碳立刻变蓝,而遇二氧化碳不反应)
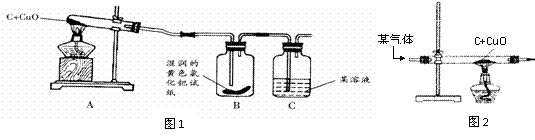
[实验结论]设计的实验装置(如下图1):
|
实验现象 |
实验结论 |
|
A中固体由黑色变成红色 |
有Cu生成 |
|
B中黄色试纸变蓝 |
有 ⑤▲ 生成 |
|
C中 ⑥▲ |
有CO2生成 |
[反思与评价]
⑴如果A装置中的试管口高于试管底部,在实验过程中可能造成的后果是 ⑦▲ 。
⑵实验结束时,为防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的橡皮塞取下,因此若没有B试剂瓶,可能导致的后果是 ⑧▲ 。
⑶根据实验结论,从环保的角度考虑,上述装置C后应添加的装置是 ⑨▲ 。
[拓展与交流]
如果用如图2装置代替图1中的A装置,这样既可以排尽试管中的空气,又能将反应产生的气体都“赶”出来,该气体可能是 ⑩▲ 。
 ⑴北京奥运会需要大量的材料。下列应用中主要使用金属材料的是 ▲
(填序号,下同),主要使用有机高分子材料的是 ▲ ;
⑴北京奥运会需要大量的材料。下列应用中主要使用金属材料的是 ▲
(填序号,下同),主要使用有机高分子材料的是 ▲ ;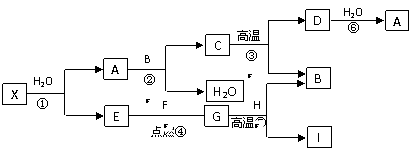 (6分)学习化学要求熟悉物质的性质以及物质之间的相互转化。含钙氧化物X是一种安全无毒的物质,常用于长途运输时鲜活鱼的供养剂。已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是冶炼得到目前使用最广泛的金属I的反应,B、E、G是常见的气体,E、F是非金属单质,F为黑色固体,B能使澄清石灰水变浑浊。回答下列问题:
(6分)学习化学要求熟悉物质的性质以及物质之间的相互转化。含钙氧化物X是一种安全无毒的物质,常用于长途运输时鲜活鱼的供养剂。已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是冶炼得到目前使用最广泛的金属I的反应,B、E、G是常见的气体,E、F是非金属单质,F为黑色固体,B能使澄清石灰水变浑浊。回答下列问题: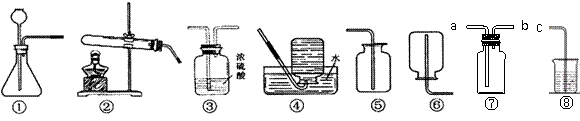 某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与。
某兴趣小组欲在实验室利用如下图所示的装置研究“碳铵”的部分性质,请你一起参与。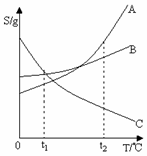 ⑶将袋内物质加入一定量的CuSO4溶液中,充分反应后过滤,滤液中的溶质一定有 ▲ 。
⑶将袋内物质加入一定量的CuSO4溶液中,充分反应后过滤,滤液中的溶质一定有 ▲ 。 Si+2R,R的化学式为
Si+2R,R的化学式为