摘要:12.根据下列框图回答问题(答题时.方程式中的M.E用所对应的元素符号表示): (1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: . (2)某同学取X的溶液.酸化后加入KI.淀粉溶液.变为蓝色.写出与上述变化过程相关的离子方程式: . (3)写出Cl2将Z氧化为K2EO4的化学方程式: . [解析] 本题以简单的框图推断为背景.考查图中涉及的几个重要的氧化还原反应的方程式.离子方程式的书写以及相关物质的结构问题. (1)借助图中“红色金属到蓝色溶液 这一信息.可判断M为Cu.方程式:Cu+H2O2+H2SO4===CuSO4+2H2O, (2)借助Y遇KSCN出现红色溶液.而Y是由X氧化而来.则推知E为Fe.X为FeSO4.Y为Fe2(SO4)3.所以离子反应为:4Fe2++O2+4H+===4Fe3++2H2O,2Fe3++2I-===2Fe2++I2,(3)根据上述分析.则Z为Fe(OH)3.K2EO4为高铁酸钾.反应式为:10KOH+3Cl2+2Fe(OH)3===2K2FeO4+6KCl+8H2O. [答案] (1)Cu+H2O2+H2SO4===CuSO4+2H2O (2)4Fe2++O2+4H+===4Fe3++2H2O 2Fe3++2I-===2Fe2++I2 (3)10KOH+3Cl2+2Fe(OH)3===2K2FeO4+6KCl+8H2O
网址:http://m.1010jiajiao.com/timu3_id_87672[举报]
(2009?淮安二模)根据下列框图回答问题:

已知白色固体N中阴、阳离子具有相同的核外电子层结构.
(1)请写出M与N反应的离子方程式:
(2)写出由A在空气中锻烧的化学方程式
(3)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式
(4)类似上述框图中A、B、C之间的转化关系一般可以表示为(副产物已略去):

则下列说法正确的是
a.若A是非金属单质,则C与水反应的生成物可能是强酸或弱酸
b.若A是金属单质,则C与水反应的生成物可能是强碱
c.若A是化合物,则C与水反应的生成物可能是强酸
d.若X是强碱,则C可能是正盐或酸式盐.
查看习题详情和答案>>

已知白色固体N中阴、阳离子具有相同的核外电子层结构.
(1)请写出M与N反应的离子方程式:
Fe 2++S 2-=FeS↓
Fe 2++S 2-=FeS↓
.(2)写出由A在空气中锻烧的化学方程式
4FeS+7O2
2Fe2O3+4SO2
| ||
4FeS+7O2
2Fe2O3+4SO2
.
| ||
(3)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式
2Fe 3++SO2+2H2O=2Fe 2++SO4 2-+4H+
2Fe 3++SO2+2H2O=2Fe 2++SO4 2-+4H+
.(4)类似上述框图中A、B、C之间的转化关系一般可以表示为(副产物已略去):

则下列说法正确的是
abcd
abcd
a.若A是非金属单质,则C与水反应的生成物可能是强酸或弱酸
b.若A是金属单质,则C与水反应的生成物可能是强碱
c.若A是化合物,则C与水反应的生成物可能是强酸
d.若X是强碱,则C可能是正盐或酸式盐.
已知:H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应.根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)
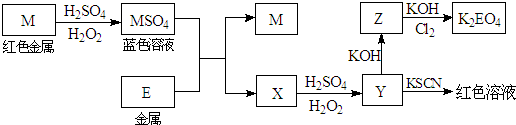
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: .
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色.分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式: 、 .
(3)写出Y到Z变化过程的离子方程式: .
(4)写出Cl2将Z氧化为K2EO4的化学方程式: .
查看习题详情和答案>>

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色.分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式:
(3)写出Y到Z变化过程的离子方程式:
(4)写出Cl2将Z氧化为K2EO4的化学方程式:
根据下列框图回答问题:

已知:化合物A的组成中含有六个结晶水,A、B均溶于水,G是一种重要化工原料.(图中部分反应物或生成物已略去).
(1)写出晶体A的化学式:
 .
.
(2)写出C→D+E反应的化学方程式:
(3)写出气体I通入H的溶液中反应的离子方程式:
(4)某同学取H的溶液,通入气体D,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式:
查看习题详情和答案>>

已知:化合物A的组成中含有六个结晶水,A、B均溶于水,G是一种重要化工原料.(图中部分反应物或生成物已略去).
(1)写出晶体A的化学式:
(NH4)2Fe(SO4)2?6H2O
(NH4)2Fe(SO4)2?6H2O
; 物质B的电子式:

(2)写出C→D+E反应的化学方程式:
4FeS+7O2
2Fe2O3+4SO2
| ||
4FeS+7O2
2Fe2O3+4SO2
.
| ||
(3)写出气体I通入H的溶液中反应的离子方程式:
Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
;(4)某同学取H的溶液,通入气体D,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式:
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
. (2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
Cu+H2O2+H2SO4═CuSO4+2H2O
Cu+H2O2+H2SO4═CuSO4+2H2O
.(2)某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色.写出与上述变化过程相关的离子方程式:
4Fe2++O2+4H+═4Fe3++2H2O
4Fe2++O2+4H+═4Fe3++2H2O
、2Fe3++2I-═2Fe2++I2
2Fe3++2I-═2Fe2++I2
.(3)写出Cl2将Z氧化为K2EO4的化学方程式:
10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O
10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O
.(4)由E制备的E(C5H5)2的结构如图,其中氢原子的化学环境完全相同.但早期人们却错误地认为它的结构为:
 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有1
1
种峰(即有几种化学环境完全相同H原子),错误的结构有3
3
种峰.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示)

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
(2)某同学取X的溶液,酸化后通入氧气再加入KI、淀粉溶液,变为蓝色,写出与上述变化过程相关的离子方程式:
(3)写出Cl2将Z氧化为K2EO4的化学方程式:
查看习题详情和答案>>

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
Cu+H2SO4+H2O2=CuSO4+2H2O
Cu+H2SO4+H2O2=CuSO4+2H2O
.(2)某同学取X的溶液,酸化后通入氧气再加入KI、淀粉溶液,变为蓝色,写出与上述变化过程相关的离子方程式:
4Fe2++4H++O2=4Fe3++2H2O
4Fe2++4H++O2=4Fe3++2H2O
、2Fe3++2I-=2Fe2++I2
2Fe3++2I-=2Fe2++I2
.(3)写出Cl2将Z氧化为K2EO4的化学方程式:
2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O
2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O
.