摘要:26. (1)Zn2++ 4OH-==[Zn(OH)4]2-, (2)10-171.80, (5)A B C D (3分.写对1个得0分.写对2个得1分.写对3个得2分.漏1个扣1分.扣完为止).
网址:http://m.1010jiajiao.com/timu3_id_48431[举报]
某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+离子.以下是某学习小组的同学设计的除去上述金属离子,回收绿矾、皓矾(ZnSO4?7H2O)和汞的探究方案.
已知:KSP(FeS)=6.3×10-18mol2?L-2,KSP(HgS)=6.4×10-53mol2?L-2KSP(ZnS)=1.6×10-24mol2?L-2
药品:NaOH溶液、Na2S溶液、稀硫酸、铁粉 稀硝酸、稀盐酸
[实验方案]
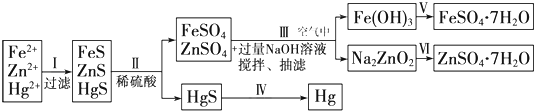
[问题探究]
(1)步骤Ⅰ中加入Na2S溶液时,三种金属离子形成沉淀的先后顺序为 .
(2)步骤Ⅱ中FeS溶解的离子方程式: .
(3)步骤Ⅲ中涉及反应的离子方程式 Zn2++4OH-═ZnO
+2H2O和 .
(4)步骤Ⅲ和步骤Ⅵ发生的相关反应,说明Zn(OH)2属于 _.
(5)欲实现步骤Ⅴ,需加入的试剂为 、 .步骤Ⅴ中从FeSO4溶液浓缩结晶得到FeSO4?7H2O时,需加稀硫酸的原因是 .
(6)步骤Ⅳ常用的方法是加热法,但在空气中加热HgS 会污染环境,其原因可能 .
查看习题详情和答案>>
已知:KSP(FeS)=6.3×10-18mol2?L-2,KSP(HgS)=6.4×10-53mol2?L-2KSP(ZnS)=1.6×10-24mol2?L-2
药品:NaOH溶液、Na2S溶液、稀硫酸、铁粉 稀硝酸、稀盐酸
[实验方案]

[问题探究]
(1)步骤Ⅰ中加入Na2S溶液时,三种金属离子形成沉淀的先后顺序为
(2)步骤Ⅱ中FeS溶解的离子方程式:
(3)步骤Ⅲ中涉及反应的离子方程式 Zn2++4OH-═ZnO
2- 2 |
(4)步骤Ⅲ和步骤Ⅵ发生的相关反应,说明Zn(OH)2属于
(5)欲实现步骤Ⅴ,需加入的试剂为
(6)步骤Ⅳ常用的方法是加热法,但在空气中加热HgS 会污染环境,其原因可能
(2010?启东市模拟)在水溶液中高价金属离子如:Fe3+、Al3+等会发生强烈水解,同样二价金属离子如Cu2+、Pb2+、Zn2+等离子在一定的pH范围内也可以水解.金属氢氧化物的沉淀直接受溶液pH的控制,利用这一方法可以除去工业污水中的某些金属离子.下图是Zn(OH)2的在某温度时的沉淀区域曲线图
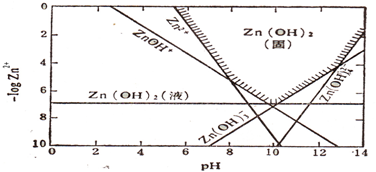
请回答下列问题:
(1)向一定浓度的Zn2+的溶液中加入足量的NaOH固体,下列说法正确的是
A、一定产生沉淀 B、先产生沉淀,后沉淀消失
C、一定不产生沉淀 D、可能不产生沉淀
(2)当pH=6、c(Zn2+)=0.01mol?L-1,Zn2+主要存在形式为
(3)向c(Zn2+)=1×10-5mol?L-1的溶液中加入固体NaOH到pH=10和pH=13,写出有关反应的离子方程式:①
(4)已知该温度下的Ksp[Zn(OH)2]=1×10-17,计算:当溶液中的c(Zn2+)=1×10-5mol?L-1,向溶液中加入NaOH固体,产生沉淀的pH,并对照该图判断是否真的产生沉淀?原因可能是什么?
查看习题详情和答案>>

请回答下列问题:
(1)向一定浓度的Zn2+的溶液中加入足量的NaOH固体,下列说法正确的是
D
D
A、一定产生沉淀 B、先产生沉淀,后沉淀消失
C、一定不产生沉淀 D、可能不产生沉淀
(2)当pH=6、c(Zn2+)=0.01mol?L-1,Zn2+主要存在形式为
ZnOH+
ZnOH+
、Zn(OH)2液体
Zn(OH)2液体
.(3)向c(Zn2+)=1×10-5mol?L-1的溶液中加入固体NaOH到pH=10和pH=13,写出有关反应的离子方程式:①
Zn2++2OH-═Zn(OH)2↓
Zn2++2OH-═Zn(OH)2↓
;②Zn2++4OH-═Zn(OH)2-4
Zn2++4OH-═Zn(OH)2-4
(4)已知该温度下的Ksp[Zn(OH)2]=1×10-17,计算:当溶液中的c(Zn2+)=1×10-5mol?L-1,向溶液中加入NaOH固体,产生沉淀的pH,并对照该图判断是否真的产生沉淀?原因可能是什么?
(2009?宿迁模拟)某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子.以下是化学研究性学习小组的同学对该厂污水处理的设想.
[资料获悉]部分阳离子以氢氧化物或硫化物形式完全沉淀时溶液的pH及硫化物的KSP如下表所示.
[探究思路]设想(一):重点是治理污染,低成本除去重金属离子Zn2+、Hg2+.
设想(二):除去污水中金属离子,回收绿矾、皓矾(ZnSO4?7H2O)和汞.
[药 品]NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉.
[实验探究](1)为了实现设想(一),甲、乙、丙三位同学分别对废水采取以下措施:
甲:加入NaOH溶液,调节溶液pH至10;
乙:加入硫化钠溶液,调节溶液pH至5;
丙:加入硫化亚铁粉末,搅拌.
你认为合理的是
(2)研究性学习小组根据设想(二)设计了如图所示的实验方案.
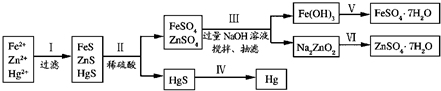
请回答:
①步骤Ⅲ中抽滤的目的是
该步骤涉及反应的离子方程式有Zn2++4OH-=ZnO22-+2H2O和
②欲实现步骤Ⅴ,所需加入的试剂有
查看习题详情和答案>>
[资料获悉]部分阳离子以氢氧化物或硫化物形式完全沉淀时溶液的pH及硫化物的KSP如下表所示.
| 沉淀物 | Fe(OH)2 | Zn(OH)2 | Hg(OH)2 |
| 沉淀完全的pH | 9.7 | 8.0 | 5.3 |
| 沉淀物 | FeS | ZnS | HgS |
| 沉淀完全的pH | ≥4.92 | ≥2.72 | ≥2.5 |
| KSP | 3.7×10-19 | 1.2×10-23 | 4×10-53 |
设想(二):除去污水中金属离子,回收绿矾、皓矾(ZnSO4?7H2O)和汞.
[药 品]NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉.
[实验探究](1)为了实现设想(一),甲、乙、丙三位同学分别对废水采取以下措施:
甲:加入NaOH溶液,调节溶液pH至10;
乙:加入硫化钠溶液,调节溶液pH至5;
丙:加入硫化亚铁粉末,搅拌.
你认为合理的是
丙
丙
(填“甲”、“乙”或“丙”),理由是硫化亚铁成本低,使沉淀转化成HgS、ZnS沉淀而除去
硫化亚铁成本低,使沉淀转化成HgS、ZnS沉淀而除去
.(2)研究性学习小组根据设想(二)设计了如图所示的实验方案.

请回答:
①步骤Ⅲ中抽滤的目的是
加快过滤速度
加快过滤速度
,抽滤的主要仪器是布氏漏斗、吸滤瓶
布氏漏斗、吸滤瓶
.该步骤涉及反应的离子方程式有Zn2++4OH-=ZnO22-+2H2O和
4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓
4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓
.②欲实现步骤Ⅴ,所需加入的试剂有
稀硫酸
稀硫酸
、铁粉(过量)
铁粉(过量)
,所涉及的主要操作依次为溶解
溶解
、过滤、重结晶
重结晶
.(2011?临川区模拟)现代炼锌的方法可分为火法和湿法两大类,镉是生产硫酸锌的副产品,属于高毒性金属,试回答下列相关问题.
(1)火法炼锌是将闪锌矿(主要含ZnS)通过浮选.焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1373-1573K,使锌蒸馏出来.主要反应为:
2ZnS+3O2
2ZnO+2SO2; 鼓风炉中:2C+O2
2CO ZnO+CO
Zn+CO2
从火法炼锌蒸馏后的残渣中含多种金属单质及In2O3,可用硫酸提取铟,某研究机构对此研究数据如下.实验中涉及的酸度(每升溶液中含硫酸的质量)与铟的浸出率如图1;硫酸溶液的体积与固体的体积比如图2
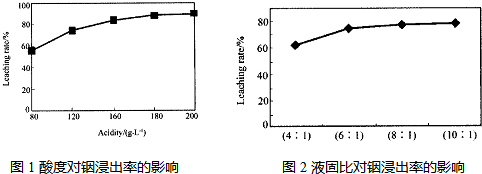
①当酸度为196时,其物质的量浓度为
②从节约原料和浸出率考虑,适宜的酸度和液固比分别为:
(2)湿法炼锌的主要工艺流程为:

①从保护环境和充分利用原料角度,如何处理或利用烟气
②除去酸浸出液中的铁,可用H2O2氧化,再调节pH使之形成Fe(OH)3沉淀,写出H2O2氧化Fe2+的离子方程式
③酸浸出液还含有Cd2+,为了防止镉污染并回收镉,根据它们性质的差异,可用氢氧化钠溶液分离,已知Zn(OH)2和氢氧化铝一样也具有两性,试写出分离的离子方程式
查看习题详情和答案>>
(1)火法炼锌是将闪锌矿(主要含ZnS)通过浮选.焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1373-1573K,使锌蒸馏出来.主要反应为:
2ZnS+3O2
| ||
| ||
| ||
从火法炼锌蒸馏后的残渣中含多种金属单质及In2O3,可用硫酸提取铟,某研究机构对此研究数据如下.实验中涉及的酸度(每升溶液中含硫酸的质量)与铟的浸出率如图1;硫酸溶液的体积与固体的体积比如图2

①当酸度为196时,其物质的量浓度为
2mol?L-1
2mol?L-1
.②从节约原料和浸出率考虑,适宜的酸度和液固比分别为:
180
180
,6:1
6:1
.(2)湿法炼锌的主要工艺流程为:

①从保护环境和充分利用原料角度,如何处理或利用烟气
将烟道气净化,用于生产硫酸等
将烟道气净化,用于生产硫酸等
.②除去酸浸出液中的铁,可用H2O2氧化,再调节pH使之形成Fe(OH)3沉淀,写出H2O2氧化Fe2+的离子方程式
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.③酸浸出液还含有Cd2+,为了防止镉污染并回收镉,根据它们性质的差异,可用氢氧化钠溶液分离,已知Zn(OH)2和氢氧化铝一样也具有两性,试写出分离的离子方程式
Cd2++2OH-=Cd(OH)2↓;Zn2++4OH-=ZnO22-+2H2O[或Zn2++4OH-=Zn(OH)42-]
Cd2++2OH-=Cd(OH)2↓;Zn2++4OH-=ZnO22-+2H2O[或Zn2++4OH-=Zn(OH)42-]
.X、Y、Z、M是由短周期元素组成的化合物;X、Y、Z均含有钠元素,且Y、Z均含有三种元素;Z的溶液显碱性.请回答下列问题:
(1)X为淡黄色粉末,可作潜水艇的供氧剂,则X为
 .
.
(2)Y、Z、M有关实验如下表:
①Y中阴离子的结构如图所示,可以看成是SO42-中的一个O原子被S原子所替代,请写出Y与稀H2SO4反应的离子方程式:

②写出含0.1mol Z的溶液与20mL 2.5mol?L-1M的溶液反应的化学方程式:
(3)如图所示,横坐标表示常温下溶液的pH,纵坐标可表示Zn2+、[Zn(OH)4]2-浓度的对数值(lgc).请回答下列问题:

①ZnCl2溶液呈酸性的原因是
②往ZnCl2溶液中加入足量Z溶液,反应的离子方程式为:
查看习题详情和答案>>
(1)X为淡黄色粉末,可作潜水艇的供氧剂,则X为
过氧化钠
过氧化钠
.X中除钠元素外,其它元素的原子结构示意图为

(2)Y、Z、M有关实验如下表:
| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |
S2O32-+2H+═S↓+SO2↑+H2O
S2O32-+2H+═S↓+SO2↑+H2O
.
②写出含0.1mol Z的溶液与20mL 2.5mol?L-1M的溶液反应的化学方程式:
AlCl3+3NaOH=Al(OH)3 ↓+3NaCl
AlCl3+3NaOH=Al(OH)3 ↓+3NaCl
.(3)如图所示,横坐标表示常温下溶液的pH,纵坐标可表示Zn2+、[Zn(OH)4]2-浓度的对数值(lgc).请回答下列问题:

①ZnCl2溶液呈酸性的原因是
Zn2++2H2O
Zn(OH)2+2H+
| 水解 |
Zn2++2H2O
Zn(OH)2+2H+
.(用离子方程式表示)| 水解 |
②往ZnCl2溶液中加入足量Z溶液,反应的离子方程式为:
Zn2++4OH-═[Zn(OH)4]2-
Zn2++4OH-═[Zn(OH)4]2-
.从图中数据可计算常温下Zn(OH)2的KSP为10-17
10-17
.