题目内容
(2009?宿迁模拟)某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子.以下是化学研究性学习小组的同学对该厂污水处理的设想.
[资料获悉]部分阳离子以氢氧化物或硫化物形式完全沉淀时溶液的pH及硫化物的KSP如下表所示.
[探究思路]设想(一):重点是治理污染,低成本除去重金属离子Zn2+、Hg2+.
设想(二):除去污水中金属离子,回收绿矾、皓矾(ZnSO4?7H2O)和汞.
[药 品]NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉.
[实验探究](1)为了实现设想(一),甲、乙、丙三位同学分别对废水采取以下措施:
甲:加入NaOH溶液,调节溶液pH至10;
乙:加入硫化钠溶液,调节溶液pH至5;
丙:加入硫化亚铁粉末,搅拌.
你认为合理的是
(2)研究性学习小组根据设想(二)设计了如图所示的实验方案.
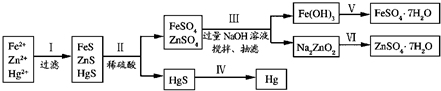
请回答:
①步骤Ⅲ中抽滤的目的是
该步骤涉及反应的离子方程式有Zn2++4OH-=ZnO22-+2H2O和
②欲实现步骤Ⅴ,所需加入的试剂有
[资料获悉]部分阳离子以氢氧化物或硫化物形式完全沉淀时溶液的pH及硫化物的KSP如下表所示.
| 沉淀物 | Fe(OH)2 | Zn(OH)2 | Hg(OH)2 |
| 沉淀完全的pH | 9.7 | 8.0 | 5.3 |
| 沉淀物 | FeS | ZnS | HgS |
| 沉淀完全的pH | ≥4.92 | ≥2.72 | ≥2.5 |
| KSP | 3.7×10-19 | 1.2×10-23 | 4×10-53 |
设想(二):除去污水中金属离子,回收绿矾、皓矾(ZnSO4?7H2O)和汞.
[药 品]NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉.
[实验探究](1)为了实现设想(一),甲、乙、丙三位同学分别对废水采取以下措施:
甲:加入NaOH溶液,调节溶液pH至10;
乙:加入硫化钠溶液,调节溶液pH至5;
丙:加入硫化亚铁粉末,搅拌.
你认为合理的是
丙
丙
(填“甲”、“乙”或“丙”),理由是硫化亚铁成本低,使沉淀转化成HgS、ZnS沉淀而除去
硫化亚铁成本低,使沉淀转化成HgS、ZnS沉淀而除去
.(2)研究性学习小组根据设想(二)设计了如图所示的实验方案.

请回答:
①步骤Ⅲ中抽滤的目的是
加快过滤速度
加快过滤速度
,抽滤的主要仪器是布氏漏斗、吸滤瓶
布氏漏斗、吸滤瓶
.该步骤涉及反应的离子方程式有Zn2++4OH-=ZnO22-+2H2O和
4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓
4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓
.②欲实现步骤Ⅴ,所需加入的试剂有
稀硫酸
稀硫酸
、铁粉(过量)
铁粉(过量)
,所涉及的主要操作依次为溶解
溶解
、过滤、重结晶
重结晶
.分析:(1)根据硫化物的Ksp判断;
(2)①抽滤速度较快;二价铁离子能与氧气在碱性条件下水解生成氢氧化铁;
②铁能将三价铁离子还原为二价铁.
(2)①抽滤速度较快;二价铁离子能与氧气在碱性条件下水解生成氢氧化铁;
②铁能将三价铁离子还原为二价铁.
解答:解:(1)沉淀总是向更难溶的方向转化,加入硫化亚铁,可以生成HgS、ZnS沉淀而除去,故答案为:丙;硫化亚铁成本低,使沉淀转化成HgS、ZnS沉淀而除去;
(2)①抽滤速度较快,抽滤的仪器有:布氏漏斗、吸滤瓶,二价铁离子能与氧气在碱性条件下水解生成氢氧化铁:4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓,故答案为:加快过滤速度;布氏漏斗、吸滤瓶;4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓;
②氢氧化铁能与稀硫酸反应生成硫酸铁,硫酸铁能与过量铁单质反应生成二价铁离子,然后溶解、过滤、重结晶得到FeSO4?7H2O,故答案为:稀硫酸;铁粉(过量);溶解;重结晶.
(2)①抽滤速度较快,抽滤的仪器有:布氏漏斗、吸滤瓶,二价铁离子能与氧气在碱性条件下水解生成氢氧化铁:4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓,故答案为:加快过滤速度;布氏漏斗、吸滤瓶;4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓;
②氢氧化铁能与稀硫酸反应生成硫酸铁,硫酸铁能与过量铁单质反应生成二价铁离子,然后溶解、过滤、重结晶得到FeSO4?7H2O,故答案为:稀硫酸;铁粉(过量);溶解;重结晶.
点评:本题考查沉淀转化、抽滤和物质的转化,题目难度不大,注意掌握抽滤的仪器及方法.

练习册系列答案
相关题目