摘要:11.K 35ClO3晶体与H 37Cl的溶液反应后.生成氯气.氯化钾和水.下列说法正确的是 A.氯化钾既不是氧化产物.也不是还原产物 B.被还原的K 35ClO3和被氧化的H 37Cl的物质的量之比为1:6 C.生成氯气的相对分子质量为72 D.每生成标准状况下的氯气11.2 L.转移的电子数为6.02×1023
网址:http://m.1010jiajiao.com/timu3_id_43974[举报]
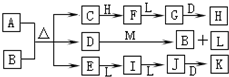 如图转化关系中,常温下E、F、L、I为无色气体,F是形成酸雨的主要原因之一,D为无色液体,M是淡黄色固体,在E的水溶液中通入过量的F得到A.
如图转化关系中,常温下E、F、L、I为无色气体,F是形成酸雨的主要原因之一,D为无色液体,M是淡黄色固体,在E的水溶液中通入过量的F得到A.试回答下列问题:
(1)A的晶体中含有的化学键为
(2)写出D→B的化学反应方程式
(3)写出E与H反应生成的正盐溶液中的离子浓度大小关系
(4)E作为燃料电池燃气时,发生的总反应为:E+O2→N2+H2O,KOH溶液为电解质溶液,负极反应式是
(5)Zn与K的稀溶液反应,当有1mol K参与反应时,有0.8mol电子转移,此时K的还原产物可能是
(6)将少量的F通入NaClO溶液中,其离子反应方程式为
铁合金及铁的化合物在生产、生活中有着重要的用途.
(1)已知铁是26号元素,写出Fe2+的电子排布式 .
(2)已知三氯化铁固体在300℃以上可升华成含二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,则该分子的结构式为 ,你认为该分子是否为平面形分子? .
(3)六氰合亚铁酸钾K4[Fe(CN)6]俗称黄血盐,它可用做显影剂,该化合物中存在的化学键类型有 (从下列选项中选填:A.离子键 B.共价键 C.金属键 D.配位键 E.氢键).黄血盐在溶液中可电离出极少量的CN-,CN-与 互为等电子体(填一种即可).CN-还可与H+结合形成一种弱酸--氢氰酸(HCN),HCN分子中碳原子的杂化轨道类型是 ,该分子的键α和π键数目分别为 .
(4)黄血盐溶液与Fe3+反应可生成一种蓝色沉淀,该物质最早由1704年英国普鲁士的一家染料厂的工人发现,因此取名为普鲁士蓝,化学式可表示为KxFey(CN)z.研究表明它的晶体的结构特征是Fe2+、Fe3+分别占据立方体的顶点,且自身互不相邻,而CN-位于立方体的棱上与Fe2+、Fe3+配位,K+填充在上述微粒形成的部分空隙中.忽略K+,该晶体的结构示意图如下四幅图所示:

根据甲图可得普鲁士蓝的化学式为 ,忽略K+,上述四幅晶体结构图中,图 是普鲁士蓝的晶胞.若把CN-看成直线,则该晶胞与《选修3》教材上的 (填化学式)的晶胞结构图高度类似.
查看习题详情和答案>>
(1)已知铁是26号元素,写出Fe2+的电子排布式
(2)已知三氯化铁固体在300℃以上可升华成含二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,则该分子的结构式为
(3)六氰合亚铁酸钾K4[Fe(CN)6]俗称黄血盐,它可用做显影剂,该化合物中存在的化学键类型有
(4)黄血盐溶液与Fe3+反应可生成一种蓝色沉淀,该物质最早由1704年英国普鲁士的一家染料厂的工人发现,因此取名为普鲁士蓝,化学式可表示为KxFey(CN)z.研究表明它的晶体的结构特征是Fe2+、Fe3+分别占据立方体的顶点,且自身互不相邻,而CN-位于立方体的棱上与Fe2+、Fe3+配位,K+填充在上述微粒形成的部分空隙中.忽略K+,该晶体的结构示意图如下四幅图所示:

根据甲图可得普鲁士蓝的化学式为
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
试回答下列问题:
(1)请写出字母O代表的元素符号
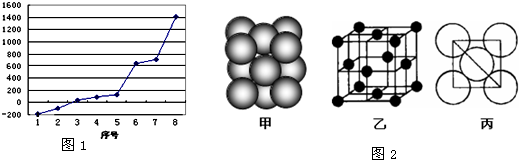
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
(4)k与l形成的化合物kl2的电子式是
 ,它在常温下呈液态,形成晶体时,属于
,它在常温下呈液态,形成晶体时,属于
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为
(用M、NA、d表示).
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式
查看习题详情和答案>>
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | ||||||||||||||||

试回答下列问题:
(1)请写出字母O代表的元素符号
Fe
Fe
,该元素在周期表中的位置第四周期第 VIII族
第四周期第 VIII族
.(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表
Si
Si
(填元素符号);其中电负性最大的是2
2
(填如图1中的序号).(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
SiC
SiC
(填化学式),试从结构角度加以解释:因SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
因SiC晶体与晶体Si都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
.(4)k与l形成的化合物kl2的电子式是


分子
分子
晶体.(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为
4
4
,该晶体的密度_
| ||
| 8NAd3 |
| ||
| 8NAd3 |
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式
NH4++Al3++5OH-+2SO42-+2Ba2+=NH3↑+3H2O+AlO2-+2BaSO4↓
NH4++Al3++5OH-+2SO42-+2Ba2+=NH3↑+3H2O+AlO2-+2BaSO4↓
.下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.

试回答下列问题:
(1)第三周期8种元素单质熔点高低顺序如图1,其中序号“8”代表
(2)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
(3)元素c的一种氧化物与元素d的一种氧化物互为等电子体,元素c的氧化物分子式是
(4)i单质晶体中原子的堆积方式如图2甲所示(面心立体最密堆积),其晶胞特征如图2乙所示.则晶胞中i原子的配位数为
查看习题详情和答案>>
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o |

试回答下列问题:
(1)第三周期8种元素单质熔点高低顺序如图1,其中序号“8”代表
Si
Si
(填元素符号);(2)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
SiC
SiC
(填化学式),试从结构角度加以解释:因SiC晶体与Si晶体都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
因SiC晶体与Si晶体都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
.(3)元素c的一种氧化物与元素d的一种氧化物互为等电子体,元素c的氧化物分子式是
CO2
CO2
,该分子是由极性
极性
键构成的非极性
非极性
分子(填“极性”或“非极性”);元素d的氧化物的分子式是N2O
N2O
.(4)i单质晶体中原子的堆积方式如图2甲所示(面心立体最密堆积),其晶胞特征如图2乙所示.则晶胞中i原子的配位数为
12
12
,一个晶胞中i原子的数目为4
4
;晶胞中存在两种空隙,分别是正四面体空隙
正四面体空隙
、正八面体空隙
正八面体空隙
.
已知B、D为常见金属单质,H常温下为无色液体,F为黑色晶体。根据下列框图所示,试回答:
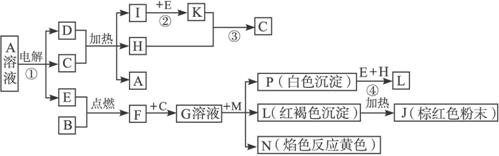
(1)写出化学式:H___________、L___________。
(2)反应①的离子方程式_____________________________________。
(3)反应②的发生,工业上采取常压操作,理由是____________________________________,对于反应③,工业上采取的操作不是使K直接与H反应,而是采用_______________________。
(4)写出反应④的化学反应方程式________________________________________________。
查看习题详情和答案>>