题目内容
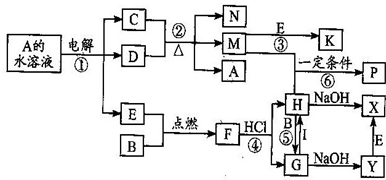
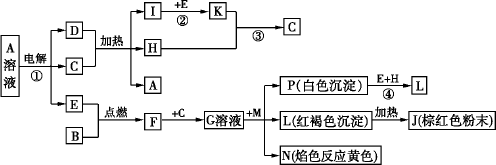
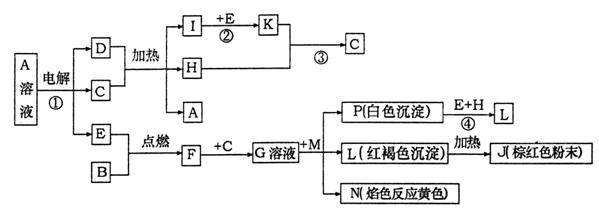
已知B、D为常见金属单质,H常温下为无色液体,F为黑色晶体。根据下列框图所示,试回答:
(1)写出化学式:H___________、L___________。
(2)反应①的离子方程式_____________________________________。
(3)反应②的发生,工业上采取常压操作,理由是____________________________________,对于反应③,工业上采取的操作不是使K直接与H反应,而是采用_______________________。
(4)写出反应④的化学反应方程式________________________________________________。
(1)H2O Fe(OH)3
(2)2Cu2++2H2O![]() 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
(3)常压下SO2的转化率已经很高 98.3%的浓硫酸吸收SO3
(4)4Fe(OH)2+O2+2H2O====4Fe(OH)3
解析:此题是无机框图推断题,综合考查了元素化合物、物质之间的转化和电解池原理的知识。题目的“题眼”是F为黑色晶体,经过多步转化生成红褐色沉淀L,加热后可得到棕红色粉末J。可以推断出J为Fe2O3,L为Fe(OH)3,F是Fe3O4,金属单质B与E点燃反应生成Fe3O4,则B是铁,E是O2;H常温下是无色液体,白色沉淀P与氧气和H反应生成Fe(OH)3,则P是Fe(OH)2,H为H2O,Fe3O4与C反应生成G溶液,则C应是酸,A溶液电解生成常见金属D、氧气和酸C,根据电解反应离子放电顺序可知D为Cu,A是铜的含氧酸盐,铜能与酸C在加热时反应,则C为浓硫酸或硝酸,结合反应②可以确定C为硫酸,I为SO2,K是SO3,反应②即SO2反应生成SO3,在常压下SO2转化率已经很高,所以工业上常采取常压操作,对于反应③即工业上制备硫酸时不用水直接吸收SO3而是用98.3%的浓硫酸吸收SO3。