摘要:为了预防碘缺乏病.国家规定每千克食盐中应含有40 mg~50 mg的碘酸钾.为检验某种食盐是否为合格的加碘食盐.某同学取食盐样品428 g.加水溶解.将得到的溶液用足量的稀硫酸酸化并加入足量的碘化钾淀粉溶液.溶液呈蓝色.再将该溶液用0.03 mol·L-1的硫代硫酸钠溶液滴定.当消耗18.00 mL硫代硫酸钠溶液时.溶液的蓝色刚好褪去.反应的离子方程式是I2+=2I-+. (1)用淀粉碘化钾溶液和稀硫酸可定性检验出食盐中的 .配平离子方程式. + I-+ H+= I2+ H2O (2)若要检验食盐中是否含有K+.实验操作是 . (3)工业上用石墨和铁为电极电解KI溶液制取KIO3.电解时.铁做 . 石墨电极上的电极反应式是 .电解过程中铁电极附近溶液的pH (填“变大 .“变小 或“不变 ). (4)该食盐样品中KIO3的含量是 mg·kg-1. 北京市西城区抽样测试 高三化学试卷答案及评分标准 2009.1
网址:http://m.1010jiajiao.com/timu3_id_396775[举报]
为了预防碘缺乏病,国家规定每千克食盐中应含有40mg~50mg的碘酸钾.为检验某种食盐是否是加碘的合格食盐,某同学取食盐样品428g,设法溶解出其中全部的碘酸钾.将溶液酸化并加入足量的碘化钾-淀粉溶液,溶液呈蓝色,再用0.030mol/L的硫代硫酸钠溶液滴定,用去18.00mL时蓝色刚好褪去.试通过计算说明该加碘食盐是否为合格产品.有关反应如下:
IO3-+5I-+6H+=3I2+3H2O
I2+2S2O32-=2I-+S4O62-.
查看习题详情和答案>>
IO3-+5I-+6H+=3I2+3H2O
I2+2S2O32-=2I-+S4O62-.
为了预防碘缺乏病,国家规定每千克食盐中应含有40mg~50mg的碘酸钾。为检验某食盐是否为合格的加碘食盐,某同学取该食盐样品428g,设法溶解出其中全部的碘酸钾,将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用0.030mol?L-1的硫代硫酸钠溶液滴定,用去18.00mL时蓝色刚好褪去。试通过计算说明该加碘食盐是否为合格产品(有关化学方程式为: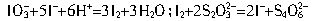 )。
查看习题详情和答案>>
)。
查看习题详情和答案>>
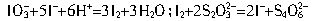 )。
查看习题详情和答案>>
)。
查看习题详情和答案>>
为了预防碘缺乏病,国家规定每千克食盐中应含有40~50mg的碘酸钾。为检验某种食盐是否为加碘的合格食盐,某同学取食盐样品428g ,设法溶解出其中全部的碘酸钾,将溶液酸化并加入足量的碘化钾淀粉溶液,溶液呈蓝色,再用0.030mol·L-1的硫代硫酸钠溶液滴定,用去18.00mL时蓝色刚好褪去。试通过计算说明该加碘食盐是否为合格产品。有关反应如下:
![]() +5I-+6H+
+5I-+6H+ ![]() 3I2+3H2O
3I2+3H2O
I2+2![]()
![]() 2I-+
2I-+![]()