网址:http://m.1010jiajiao.com/timu3_id_391144[举报]
(1)写出H2在高温下还原CuO过程中可能发生反应的化学方程式。
①CuO+H2![]() Cu+H2O,②____________________________________,
Cu+H2O,②____________________________________,
③________________________________________________________________。
(2)Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸和稀硝酸四种试剂。简述如何用最简便的实验方法来检验CuO经氢气还原所得到的红色产物中是否含有Cu2O。
____________________________________________________________________。
(3)若将
(4)若有a g CuO和Cu2O的混合物,加入2.0 mol·L-1 H2SO4 V mL,使混合物恰好全部反应,则V的取值范围为________________________________________________。
查看习题详情和答案>>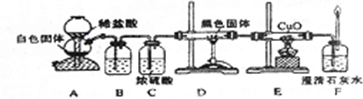
已知:C+H2O
| ||
| ||
| ||
试回答下列问题:
①装置B中最适宜的试剂是
②根据该实验中的
③若要根据装置P中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置
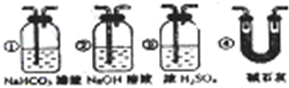

请同答下列问题:
(1)烧瓶中装入的试剂是锌粒,其中将发生反应的离子方程式是
(2)试剂C是水,其作用是
(3)试剂D是
(4)连接好装置后的实验操作依次是
①检验氢气纯度 ②加热E ③检验装置气密性
④点燃G管溢出的气体 ⑤从A瓶逐滴滴加液体
(5)从实验中测得了下列数据:
①空E管的质量a;
②E管和试样的总质量b;
④反应后E管和内盛物的总质量c(冷却到室温称量);
④反应前F管及内盛物的总质量d;
⑤反应后F管及内盛物的总质量e.
由以上数据可以列出计算混合粉末中铜元素的质量分数的两个不同计算式,其中较简单的是
(6)已知:C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
| ||
. |
则用炭粉在高温条件下还原CuO生成Cu2O的热化学方
(1)关于反应生成物的定量研究:
已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol?L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定
A.含Fe2+,不含Fe3+B.含Fe3+,不含Br-C.含Fe3+,含有Br-
(2)关于反应限度的研究:
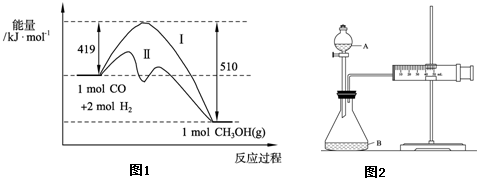
已知在773K、固定体积的容器中,反应CO(g)+2H2(g)?CH3OH(g)过程中能量变化如图1.曲线Ⅱ表示使用催化剂时的能量
变化.若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值.
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可):
(3)关于反应速率的研究:
氧化还原反应中实际上包含氧化和还原两个过程.下面是HNO3发生 的一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O
①KMnO4、Na2CO3、CuO、KI四种物质中的
②欲用图2装置测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定
(15分)纳米级Cu2 O 粉末,由于量子尺寸效应,其具有特殊的光学、电学及光电化学性质,在太阳电池、传感器、超导体、制氢和电致变色、环境中处理有机污染物等方面有着潜在的应用。
Ⅰ.纳米氧化亚铜的制备
(1)四种制取Cu2O的方法如下:
①火法还原。用炭粉在高温条件下还原CuO;
②最新实验研究用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。
已知:N2H4(l)+O2(g) N2(g)+2H2O(l)
△H=-a
kJ/mol
N2(g)+2H2O(l)
△H=-a
kJ/mol
Cu(OH)2(s) CuO(s)+H2O(l) △H=b kJ/mol
CuO(s)+H2O(l) △H=b kJ/mol
4CuO(s) 2Cu2O(s)+O2(g)
△H=c
kJ/mol
2Cu2O(s)+O2(g)
△H=c
kJ/mol
则该方法制备Cu2O的热化学方程式为 。
③工业中主要采用电解法:用铜和钛作电极,电解氯化钠和氢氧化钠的混合溶液,电解总方程式为:2Cu+H2O Cu2O+H2↑,则阳极反应式为:
。
Cu2O+H2↑,则阳极反应式为:
。
④还可采用Na2SO3还原CuSO4法:将Na2SO3 和CuSO4加入溶解槽中,制成一定浓度的溶液,通入蒸气加热,于100℃~104℃间反应即可制得。写出该反应的化学方程式: 。
Ⅱ.纳米氧化亚铜的应用
(2)用制得的Cu2O进行催化分解水的实验
①一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入10. 0 mol水蒸气,发生反应:
2H2O(g)  2H2(g)+O2(g)
△H=+484 kJ·mol-1
2H2(g)+O2(g)
△H=+484 kJ·mol-1
T1温度下不同时段产生O2的量见下表:
|
时间/min |
20 |
40 |
60 |
80 |
|
n(O2)/mol |
1.0 |
1.6 |
2.0 |
2.0 |
前20 min的反应速率 v(H2O)= ;该该温度下,反应的平衡常数的表达式K= ;若T2温度下K=0.4,T1 T2(填>、<、=)
②右图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为 ,t2时改变的条件可能为 ;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为 ;

③用以上四种方法制得的Cu2O在其它条件相同下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。

A.方法③、④制得的Cu2O催化效率相对较高
B.方法④制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有
D.Cu2O催化水分解时,需要适宜的温度
查看习题详情和答案>>