摘要:19.分别取40mL的0.50mol/L盐酸与0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题. (1)理论上稀强酸.稀强碱反应生成1mol水时放出57.3kJ的热量.写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 , (2)如右图所示.仪器A的名称是 ,在实验过程中.如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度.则测得的 (填“偏大 .“偏小 或“无影响 ), (3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3.又知中和后生成溶液的比热容c=4.18J/.为了计算中和热.实验时还需测量的数据有 , A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量 C.反应前氢氧化钠溶液的温度 D.反应前氢氧化钠溶液的质量 E.反应后混合溶液的最高温度 F.反应后混合溶液的质量 (4)某学生实验记录数据如下: 实验序号 起始温度t1℃ 终止温度t2℃ 盐酸 氢氧化钠 混合溶液 1 20.0 20.1 23.2 2 20.2 20.4 23.4 3 20.5 20.6 23.6 依据该学生的实验数据计算.该实验测得的中和热= , (5) 用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液.理由是 . 650℃ 150℃ 20.胆矾在受热过程中发生如下反应: 1000℃ CuSO4·5H2O=====CuSO4+5H2O CuSO4======CuO+SO3 4CuO======2Cu2O+O2 2SO3 2SO2 + O2 取一定量硫酸铜晶体(CuSO4·XH2O)置于已知质量的坩埚中称重.测得硫酸铜晶体的质量为ag.用酒精灯将坩埚充分加热.然后放入干燥器中冷却.再称重.经若干次加热. 班级 姓名 学号 冷却称重.直到质量基本不变.称得坩埚中剩余固体物质的质量为bg. (1)在上述实验操作中.至少称量 次. (2)该晶体中x的实验值为 . (3)将实验值与根据化学式(CuSO4·5H2O)计算的结果比较.实验值大于计算值.造成误差的原因可能是 . a.实验中部分固体溅出 b.加热温度过高 c.部分样品已风化 d.硫酸铜晶体中含有不挥发性杂质 (4)另取25.0g胆矾(CuSO4·5H2O).缓慢升温到1000℃. ①在加热过程中.当固体物质的质量为10.0g时.该固体可能的组成是 . ②在1000℃时.除水外.其余气态产物物质的量(n)的取值范围是(不考虑实 验误差) .
网址:http://m.1010jiajiao.com/timu3_id_388685[举报]
分别取40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
(2)为什么中和热测定中要用稍过量的碱(或酸):
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
查看习题详情和答案>>
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
环形玻璃搅拌棒
环形玻璃搅拌棒
、量筒
量筒
.(2)为什么中和热测定中要用稍过量的碱(或酸):
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
-50.2KJ/mol
-50.2KJ/mol
; (结果保留一位小数)(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
abd
abd
.a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
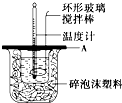 分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.(1)理论上稀强酸、稀强碱反应生成1mol 水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃).为了计算中和热,实验时还需测量的数据有(填序号)
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
| 实验 序号 |
起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 ;
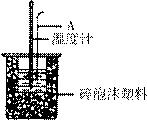 (2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃)。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=________________;(结果保留一位小数)
(4) (填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是 。
查看习题详情和答案>>
分别取40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、______、______.
(2)为什么中和热测定中要用稍过量的碱(或酸):______
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/.为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=______; (结果保留一位小数)
(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)______.
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
查看习题详情和答案>>
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、______、______.
(2)为什么中和热测定中要用稍过量的碱(或酸):______
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/.为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=______; (结果保留一位小数)
(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)______.
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
查看习题详情和答案>>
分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______.
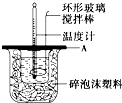
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是______;
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃).为了计算中和热,实验时还需测量的数据有(填序号)______.
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H=______.
查看习题详情和答案>>
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______.
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是______;
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃).为了计算中和热,实验时还需测量的数据有(填序号)______.
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
| 实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
