题目内容
分别取40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
(2)为什么中和热测定中要用稍过量的碱(或酸):
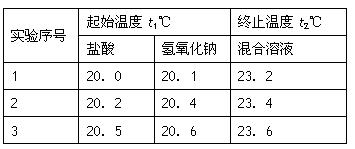
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
环形玻璃搅拌棒
环形玻璃搅拌棒
、量筒
量筒
.(2)为什么中和热测定中要用稍过量的碱(或酸):
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
-50.2KJ/mol
-50.2KJ/mol
; (结果保留一位小数)(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
abd
abd
.a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
分析:(1)根据量热计的构造和实验步骤来确定实验的仪器;
(2)在实验中,为了保证酸(或碱)能够完全被中和,往往使得一方过量;
(3)根据公式△H=Q=cm△T来计算;
(4)a.实验装置保温、隔热效果必须好;
b.量取NaOH溶液的体积时视线要和凹液面相平;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度..
(2)在实验中,为了保证酸(或碱)能够完全被中和,往往使得一方过量;
(3)根据公式△H=Q=cm△T来计算;
(4)a.实验装置保温、隔热效果必须好;
b.量取NaOH溶液的体积时视线要和凹液面相平;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度..
解答:解:(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、搅拌器以及量筒,故答案为:环形玻璃搅拌棒;量筒;
(2)在中和热测定的实验中,为了保证酸(或碱)能够完全被中和,往往使得一方过量,故答案为:为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热;
(3)40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液中,溶液质量m=80mL×1g/mL=80g,c=4 18J/(g?℃),代入公式△H=Q=cm△T得△H=Q=4.18J/(g?℃)×80g×
=-50.2KJ/mol,故答案为:-50.2KJ/mol;
(4)a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,故b正确;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c错误;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,故d正确.
故选abd.
(2)在中和热测定的实验中,为了保证酸(或碱)能够完全被中和,往往使得一方过量,故答案为:为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热;
(3)40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液中,溶液质量m=80mL×1g/mL=80g,c=4 18J/(g?℃),代入公式△H=Q=cm△T得△H=Q=4.18J/(g?℃)×80g×
| (23.2-20.1)+(23.1-20.2)+(25.3-20.5) |
| 3 |
(4)a.实验装置保温、隔热效果必须好,否则影响实验结果,故a正确;
b.量取NaOH溶液的体积时仰视读数,会导致所量的氢氧化钠体积偏大,故b正确;
c.允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c错误;
d.用温度计测定NaOH溶液起始温度后,要将温度计回零直再测定H2SO4溶液的温度,故d正确.
故选abd.
点评:本题考查热化学方程式以及反应热的计算,题目难度大,注意理解中和热的概念、把握热化学方程式的书写方法,以及测定反应热的误差等问题.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
(7分)分别取40mL的0.50 mol/L盐酸与40mL的0.55 mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1 mol 水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式__________________________________。
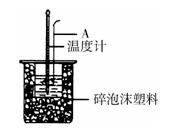
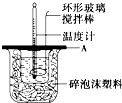
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是_____________________________________________;
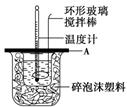
(3)假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g·℃)。为了计算中和热,实验时还需测量的数据有(填序号)________。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
|
实验 序号 |
起始温度t1/℃ |
终止温度t2/℃ |
|
|
盐酸 |
氢氧化钠 |
混合溶液 |
|
|
1 |
20.0 |
20.1 |
23.2 |
|
2 |
20.2 |
20.4 |
23.4 |
|
3 |
20.5 |
20.6 |
23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=________;
 分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
分别取40mL的0.50mol/L盐酸与40mL的0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.