摘要:7.已知25℃时.氢氟酸的电离平衡常数KaHF=3.6×10-4, CaF2的溶度积常数Ksp(CaF2)=1.46×10-10.现向1L 0.2mol·L-1HF溶液中加入1L 0.2mol·L-1CaCl2y溶液.则下列说法中.正确的是 ( ) A.25℃时.0.1mol·L-1HF 溶液中pH=2 B.Ksp(CaF2)随温度和浓度的变化而变化 C.该体系中没有沉淀产生 D.该体系中HF与CaCl2反应产生沉淀
网址:http://m.1010jiajiao.com/timu3_id_370264[举报]
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l)△H=-67.7kJ/mol,②H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,氢氟酸的电离方程式及热效应可表示为 .
(2)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量增大的是 .
A.c(H+) B.c(H+)?c(OH-) C.
D.
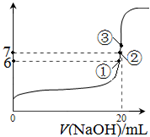
(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 .
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol/L
(4)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液.
依据数据判断pH由大到小的顺序是 .
(5)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验事实证明之 .
(6)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与水反应得到HF和化合物A,每生成1molHF转移 mol电子.
查看习题详情和答案>>
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) |
7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 |
3.0×10-8 |
(2)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量增大的是
A.c(H+) B.c(H+)?c(OH-) C.
| c(H+) |
| c(HF) |
| c(OH-) |
| c(H+) |

(3)25℃时,在20mL0.1mol/L氢氟酸中加入VmL0.1mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol/L
(4)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液.
依据数据判断pH由大到小的顺序是
(5)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验事实证明之
(6)长期以来,一直认为氟的含氧酸不存在.1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F.HFO与水反应得到HF和化合物A,每生成1molHF转移
已知25℃时,下列酸的电离常数:醋酸:1.75×10-5 氢氰酸:4.93×10-10 氢氟酸:7.2×10-4 甲酸:1.77×10-4 则物质的量浓度均为0.1mol?L-1的上述溶液酸性最强的是( )
查看习题详情和答案>>
已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图1.反应开始时,两种溶液产生CO2的速率明显不同的原因是 ;
反应结束后所得溶液中c(SCN-) c(CH3COO-)(填“>”,“=”或“<”)
(2)2.0×10-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如图2.
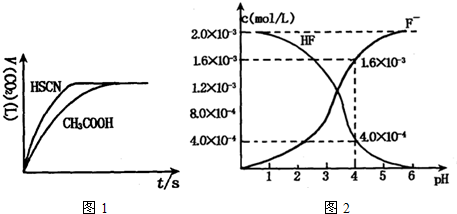
则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp=1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4mol/L的CaCl2溶液等体积混合,调节溶液pH=4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成? (填“有”或“没有”),筒述理由: .
查看习题详情和答案>>
Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图1.反应开始时,两种溶液产生CO2的速率明显不同的原因是
反应结束后所得溶液中c(SCN-)
(2)2.0×10-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如图2.

则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp=1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4mol/L的CaCl2溶液等体积混合,调节溶液pH=4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?