江西省上高二中2009届高三年级全真模拟
理综试卷
命题:廖喻萍 黎毛生 鲁卫东
一、选择题
1.篮球运动员姚明的“佳得乐”运动饮料广告词:“解口渴,更解体渴,佳得乐。”其中的“解体渴”主要是指“佳得乐”饮料中( )
A.含有大量水,补充剧烈运动散失的水分
B.含有葡萄糖,补充剧烈运动散失的能量
C.含有大量水和少量无机盐,补充剧烈运动散失的水分和无机盐
D.添加的葡萄糖和无机盐,能补充剧烈运动散失的能量和无机盐
2.下列与酵母菌有关的叙述中,正确的是( )
A.催化酵母菌酒精发酵的酶属于诱导酶
B.酵母菌细胞中ATP水解去掉2个磷酸基团后可以参与其遗传物质的构成
C.培养基中添加青霉素可以将酵母菌从大肠杆菌中分离出来
D.利用酵母菌发酵生产获得的单细胞蛋白可以用离子交换的方法提纯
3.某研究人员模拟赫尔希和蔡斯关于噬菌体侵入细菌实验,进行了以下4个实验:①用32P标记的噬菌体侵染未标记的细菌②用未标记的噬菌体侵染35S标记的细菌③用15N标记的噬菌体侵染未标记的细菌④用未标记的噬菌体侵染3H标记的细菌
以上4个实验,短时间保温后搅拌离心,检测到放射性主要部位是( )
A.沉淀、沉淀、沉淀和上清液、沉淀和上清液
B.沉淀、沉淀、沉淀和上清液、沉淀
C.沉淀、上清液、沉淀、沉淀和上清液
D.上清液、上清液、沉淀和上清液、上清液
4.高三学生小明最近到医院体检,体检报告中的肝功能检验结果显示:乙肝抗原呈阴性(-),乙肝抗体呈阳性(+)。他说自己没有注射过乙肝疫苗,就此结果向你咨询,你应该给他怎样的合理解释?(说明:“+”表示有,“-”表示没有)
A.你体内没有乙肝病毒,但含有乙肝抗体,说明你可能曾感染乙肝病毒后痊愈了 B.你体内没有乙肝病毒,但含有乙肝抗体,一定是妈妈怀孕时传递给你的免疫力
C.你体内带有乙肝抗体,说明一定也有乙肝病毒,需要到医院就诊
D.你体内没有乙肝病毒,但含有乙肝抗体,这是父母遗传给你的免疫力
5.某炭疽杆菌的A基因含有A1~A66个小段,某生物学家分离出此细菌A基因的2个缺失突变株: K(缺失A2、A3)、L(缺失A3、A4、A5、A6)。将一未知的点突变株X与L共同培养,可以得到转化出来的野生型细菌(即:6个小段都不是突变型);若将X与K共同培养,得到转化的细菌都为非野生型。由此可判断X的点突变最可能位于A基因的( )
A.A2小段 B.A3小段 C.A4小段 D.A5小段
6.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.1 mol D318O+离子中含有的中子数为10NA
B.1 mol SiO2晶体中含有的Si―O键数为2NA
C.
D.
7.下列叙述正确的是( )
A.Fe ( OH )3不溶于水不能通过化合反应直接得到
B.H2O、H2S随着相对分子质量的增大,沸点逐渐升高
C.只含一种元素的物质可能为混合物
D.物质B的饱和溶液降低温度时一定有B物质析出
8.下列反应的离子方程式正确的是
A.澄清石灰水中滴加过量的小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
B.铵明矾[NH4Al(SO4)2?12H2O]溶液中加入过量Ba(OH)2溶液:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
C.H2O2溶液中滴加酸性KMnO4溶液:
2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O
D.尼泊金酸(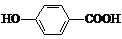 )与碳酸氢钠溶液反应:
)与碳酸氢钠溶液反应:
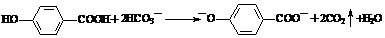
9.下列各项选项所述的两个量,前者一定大于后者的是 ( )
①HF和HBr的沸点;②纯水在
A.①②⑥⑧ B.①②③⑤ C.④⑤⑥⑦ D.①②⑥⑦
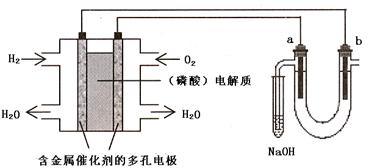
10.用酸性氢氧燃料电池电解苦卤水 (含Cl?、Br?、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是
A.电池工作时,正极反应式为:O2 +2 H2O + 4e―=4 OH?
B.电解时,a 电极周围首先放电的是Br?而不是Cl?,说明当其它条件相同时前者的还原性强于后者
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗
 11.已知
11.已知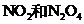 可以相互转化:
可以相互转化:
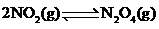 ;
;
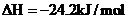 在恒温条件下,将一定
在恒温条件下,将一定
量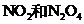 的混合气体通入一容积为
的混合气体通入一容积为
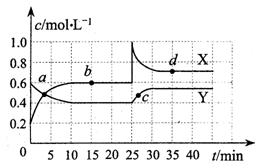
密闭容器中,反应物浓度随时间变化关系如右
图。下列说法正确的是( )
A.前10 min内用v(NO2)表示的化学反应速度为0.02mol/(L?min)
B.a、b、c、d四个点中,a、c两点的v正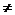 v逆
v逆
C.反应进行到10 min时放出的热量为9.68 kJ
D.25 min时,导致平衡移动的原因是将密闭容器的体积缩小为
12.下列对实验现象的解释与结论正确的是
编号
实验操作
实验现象
解释与结论
A
向鸡蛋清溶液中加入饱和(NH4)2SO4溶液
有白色沉淀产生
蛋白质发生了变性
B
向某溶液中加入BaCl2溶液
有白色沉淀产生
生成难溶于水的BaSO4,该溶液中一定含有SO42-
C
向苯中滴入少量浓溴水,振荡,静置
溶液分层,上层呈橙红色,下层几乎无色
苯和溴水发生取代反应,使溴水褪色
D
向蔗糖中加入浓硫酸
蔗糖变黑,体积膨胀,放热并放出刺激性气味气体
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等
13.某烃的组成为C15H24,分子结构非常对称,实验证明该烃中仅存在三种基团乙烯基(CH2
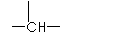 |
=CH-),亚甲基(-CH2-),和次甲基( ),并且乙烯基和次甲基之间必须通过亚甲基相连。当该烃含有单环结构时,分子中的乙烯基和亚甲基数依次为
A. 2个、3个 B . 3个、3个
C. 4个、6个 D.
3个、6个
14、太阳围绕银河系中心的运动可视为匀速圆周运动,其运动速度约为地球公转速度的7倍,轨道半径约为地球公转轨道半径的2×109倍。为了粗略估算银河纱系中恒星的数目,可认为银河系中所有恒星的质量都集中在银河系中心,且银河系中恒星的平均质量约等于太阳质量,则银河系恒星数目约为( )
A.1015 B.
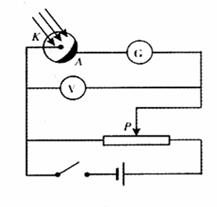 15、用下图电路可研究光电效应规律,图中标有A和K的为光电管,其中A为阴极,受光照射时可产生光电效应现象,K为阳极.理想电流计G可检测通过光电管的电流,理想电压表V.用来指示光电管两端电压.现接通电源,用光子能量为10.5eV的光照射阴极A,电流计中有读数,若将滑线变阻器的滑片P缓慢向右滑动,电流计的读数逐渐减小,当滑至某一位置时电流计的读数恰好为0,读出此时电压表的示数为6.0V;现保持滑片P的位置不变,改用光子能量为12eV的光照射阴极A,以下判断正确的是
15、用下图电路可研究光电效应规律,图中标有A和K的为光电管,其中A为阴极,受光照射时可产生光电效应现象,K为阳极.理想电流计G可检测通过光电管的电流,理想电压表V.用来指示光电管两端电压.现接通电源,用光子能量为10.5eV的光照射阴极A,电流计中有读数,若将滑线变阻器的滑片P缓慢向右滑动,电流计的读数逐渐减小,当滑至某一位置时电流计的读数恰好为0,读出此时电压表的示数为6.0V;现保持滑片P的位置不变,改用光子能量为12eV的光照射阴极A,以下判断正确的是
A.光电管阴极材料的逸出功为4.5eV
B、电流计的读数仍然为0
C、光电子的最大初动能一定变大
D、若用光子能量为9.5ev的光照射阴极A,同时把滑片P向左移动少许,电流计的读数一定不为0
16、假设在NaCl蒸气中存在由钠离子和氯离子Cl―靠静电相互作用构成的单个氯化钠NaCl分子,若取Na+与Cl―相距无限远时其电势能为零,一个NaCl分子的电势能有为 - 6.1eV,在将一个NaCl分子分解成彼此远离的中性钠原子Na和中性氯原子Cl的过程中,外界供给的总能量等于4.8eV,已知使一个中性钠原子Na最外层的电子脱离钠原子而形成钠离子Na+所需的能量(电离能)为5.1eV,则使一个中性氯原子Cl结合一个电子形成氯离子Cl―所放的能量(亲和能)是( )
A.5.1eV B.3.8 eV C.6.4eV D.5.8 eV
17、如图是一个用折射率n=2.4的透明介质做成的四棱柱镜的横截面图,其中∠A=∠C=90°,∠B=60°,在AB面上有一束垂直于它的平行光线射入,以下关于光线经过各个界面出射情况的说法正确的是( )
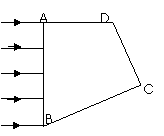 A.一定有光线垂直DC面射出
A.一定有光线垂直DC面射出
B.一定有光线垂直BC面射出
C.一定有光线垂直AB面射出
D.一定有光线垂直AD面射出
18、有一测量微小时间差的装置,是由两个摆长略有微小差别的单摆同水平悬挂构成.两个单摆摆动平面前后相互平行,现测得两单摆完成 50次全振动的时间分别为 50.0 S和 49.0 S,某同学利用此装置测量小于单摆周期的微小时间差,具体操作如下:把两摆球向右拉至相同的摆角处,先释放长摆摆球,接着再释放短摆摆球,测得短摆经过若干次全振动后,两摆恰好第一次同时同方向通过某位置,由此可得出释放两摆的微小时间差.若测得释放两摆的时间差Δt=0.165s,则下列说法正确的是( )
A.两单摆的周期差ΔT=0.02s
B.在短摆释放8.085s后,两摆恰好第一次同时向左通过平衡位置
C.在短摆释放8.085s后,两摆恰好第一次同时向右通过平衡位置
D.为了能更准确地测量微小的时间差,把两摆的摆长差增大一些
19、单冷型空调器一般用来降低室内温度,其制冷系统与冰箱制冷系统结构基本相同,某单冷型空调器的制冷机从低温物体吸热量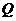 1,向高温物体放出热量
1,向高温物体放出热量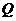 2,而外界必须对工作物质做功W,制冷系数
2,而外界必须对工作物质做功W,制冷系数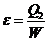 ,设某一空调的制冷系数为10,若制冷机每天从房间内部吸收
,设某一空调的制冷系数为10,若制冷机每天从房间内部吸收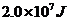 的热量,则下列说法不正确的是( )
的热量,则下列说法不正确的是( )
A.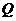 1一定大于
1一定大于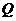 2 B.空调的制冷系数越大越节能
2 B.空调的制冷系数越大越节能
C.制冷机每天放出的热量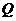 1=
1=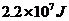
D.制冷机每天放出的热量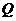 1=
1=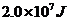
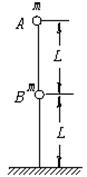 20、如图,长为2L的轻杆上端及其正中央固定两个质量为m的小球,杆竖直立在光滑的水平面上,杆原来静止,现让其自由倒下,设杆在倒下过程中着地端始终不离开地面,则A着地时的速度为( )
20、如图,长为2L的轻杆上端及其正中央固定两个质量为m的小球,杆竖直立在光滑的水平面上,杆原来静止,现让其自由倒下,设杆在倒下过程中着地端始终不离开地面,则A着地时的速度为( )
A.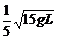 B.
B.
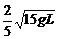
C. 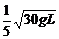 D.
D.
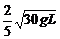
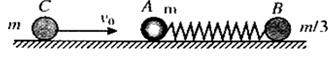
21、如图所示,光滑水平面上,质量为m的小球A和质量为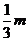 的小球B通过轻质弹簧相连并处于静止状态,弹簧处于自由伸长状态;质量为m的小球C以初速度
的小球B通过轻质弹簧相连并处于静止状态,弹簧处于自由伸长状态;质量为m的小球C以初速度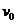 沿AB连线向右匀速运动,并与小球A发生弹性正碰。在小球B的右侧某位置固定一块弹性挡板(图中未画出)。当小球B与挡板发生正碰后立刻将挡板撤走,不计所有碰撞过程中的的机械能损失,弹簧始终处于弹性限度以内,小球B与固定挡板的碰撞时间极短,碰后小球B的速度大小不变,但方向相反,则B与挡板后弹簧弹性势能的最大值
沿AB连线向右匀速运动,并与小球A发生弹性正碰。在小球B的右侧某位置固定一块弹性挡板(图中未画出)。当小球B与挡板发生正碰后立刻将挡板撤走,不计所有碰撞过程中的的机械能损失,弹簧始终处于弹性限度以内,小球B与固定挡板的碰撞时间极短,碰后小球B的速度大小不变,但方向相反,则B与挡板后弹簧弹性势能的最大值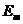 可能是( )
可能是( )
 A.
A.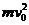 B.
B.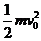
C.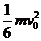 D.
D.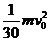
二、实验题
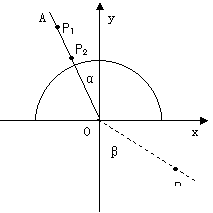 22、I、如图画有直角坐标系xOy的白纸位于水平桌面上,M是放在白纸上的半圆形玻璃砖,其底面的圆心在坐标原点,直边与x轴重合,OA是画在纸上的直线,P1、P2为竖直地插在直线OA上的两枚大头针,P3是竖直地插在纸上的第三枚大头针,α是直线OA与y轴正方向的夹角, β是直线OP3与y轴负方向的夹角,只要直线OA画得合适,且P3的位置取得正确,测得角α和β,便可求得玻璃得折射率。某学生在用上述方法测量玻璃的折射率,在他画出的直线OA上竖直插上了P1、P2两枚大头针,但在y<0的区域内,不管眼睛放在何处,都无法透过玻璃砖看到P1、P2的像,他应该采取的措施是__________________,若他已透过玻璃砖看到了P1、P2的像,确定
22、I、如图画有直角坐标系xOy的白纸位于水平桌面上,M是放在白纸上的半圆形玻璃砖,其底面的圆心在坐标原点,直边与x轴重合,OA是画在纸上的直线,P1、P2为竖直地插在直线OA上的两枚大头针,P3是竖直地插在纸上的第三枚大头针,α是直线OA与y轴正方向的夹角, β是直线OP3与y轴负方向的夹角,只要直线OA画得合适,且P3的位置取得正确,测得角α和β,便可求得玻璃得折射率。某学生在用上述方法测量玻璃的折射率,在他画出的直线OA上竖直插上了P1、P2两枚大头针,但在y<0的区域内,不管眼睛放在何处,都无法透过玻璃砖看到P1、P2的像,他应该采取的措施是__________________,若他已透过玻璃砖看到了P1、P2的像,确定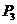 位置的方法是___________。若他已正确地测得了的
位置的方法是___________。若他已正确地测得了的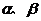 的值,则玻璃的折射率n=________
的值,则玻璃的折射率n=________
II、多用电表是实验室和生产实际常用的仪器。
①如图(甲)是一个多用电表的内部电路图,在进行电阻测量时,应将S拨到____或____; 在进行电压测量时,应将S拨到______或______;
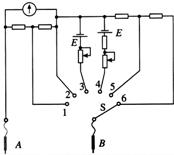
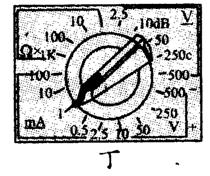
②使用多用电表进行了两次测量,指针所指的位置分别如图(乙)中a、b所示.若选择开关处在“×10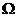 ”的电阻档时指针位于a,则被测电阻的阻值是________
”的电阻档时指针位于a,则被测电阻的阻值是________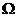 .若选择开关处在“直流电压2.5V”档时指针位于b,则被测电压是________V.
.若选择开关处在“直流电压2.5V”档时指针位于b,则被测电压是________V.
 |
 |
||
甲 乙
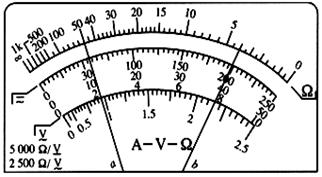
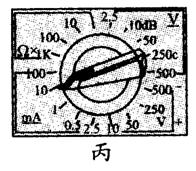
③两位同学使用完多用电表后,分别把选择开关置于图丙和 图丁位置,你认为图____ 的位置比较好.
 |
 |
||
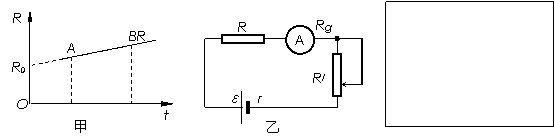
(2)(甲)表示某电阻R随摄氏温度t变化的关系,图中R0表示0℃时的电阻,K表示图线的斜率 .若用该电阻与电池(E,r)、电流表Rg、变阻器R′串连起来,连接成如图(乙)所示的电路,用该电阻做测温探头,把电流表的电流刻度改为相应的温度刻度,于是就得到了一个简单的“电阻测温计”.
①实际使用时要把电流表的刻度值改为相应的温度刻度值,若温度t1<t2,则t1的刻度应在t2的 侧(填“左”、“右”);
②在标识“电阻测温计”的温度刻度时,需要弄清所测温度和电流的对应关系。请用E、R0、K等物理量表示所测温度t与电流I的关系式:t= ;
③由②知,计算温度和电流的对应关系,需要测量电流表的内阻(约为200Ω).已知实验室有下列器材:A. 电阻箱(0-99.99Ω);B. 电阻箱(0-999.9Ω);C. 滑线变阻器(0-20Ω);D. 滑线变阻器(0-20kΩ).此外,还有电动势合适的电源、开关、导线等.
请在方框内设计一个用“半偏法”测电流表内阻Rg的电路;
在这个实验电路中,电阻箱应选 ;滑线变阻器应选 .(只填代码)
 三、计算题
三、计算题
23、(16分)如图所示的木板由倾斜部分和水平部分组成,两部分之间由一段圆弧面相连接,在木板的中间有位于竖直面内的光滑圆槽轨道,斜面的倾角为θ.现有10个质量均为m 、半径均为r的均匀刚性球,在施加于1号球的水平外力F的作用下均静止,力F与圆槽在同一竖直面内,此时1号球球心距它在水平槽运动时的球心高度差为h.现撤去力F使小球开始运动,直到所有小球均运动到水平槽内.重力加速度为g.求:
⑴水平外力F的大小;⑵1号球刚运动到水平槽时的速度;
⑶整个运动过程中,2号球对1号球所做的功.
24、(18分)如图甲所示,“月”字形轨道的每一短边的长度都等于a,只有三根平行的短边有电阻,阻值都是r,不计其它各边电阻。使导轨平面与水平面成夹角θ固定放置,如图乙所示。一根质量为m的条形磁铁,其横截面是边长为a的正方形,磁铁与导轨间的摩擦不计,磁铁与导轨间绝缘。假定导轨区域内的磁场全部集中在磁铁的端面,并可近似为匀强磁场,磁感应强度为B,方向垂直导轨平面。开始时让磁铁从轨道上某一位置由静止下滑,使磁铁恰能匀速进入正方形2。在磁铁从开始运动到其端面与正方形1重合的过程中,求:(已知重力加速度为g)
(1)磁铁下滑时离正方形2上边的距离S;
 (2)上述过程中通过MN边的感应电荷量q;
(2)上述过程中通过MN边的感应电荷量q;
(3)上述过程中所有电阻产生的热量Q。
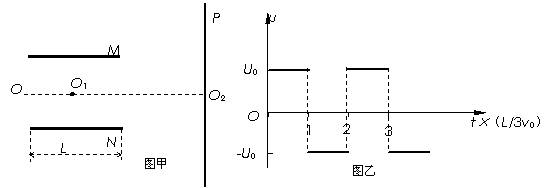
25、(20分)如图甲所示,M和N是相互平行的金属板,OO1O2为中线,O1为板间区域的中点,P是足够大的荧光屏.带电粒子连续地从O点沿OO1方向射入两板间.
(1)若两板间只存在一个以O1点为圆心的圆形匀强磁场区域,磁场方向垂直纸面向里,已知磁感应强度B=0.50T,两板间距d=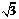 cm,板长L=1.0cm,带电粒子质量m=2.0×10-25kg,电量q=8.0×10-18C,入射速度v =
cm,板长L=1.0cm,带电粒子质量m=2.0×10-25kg,电量q=8.0×10-18C,入射速度v =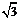 ×105m/s.若能在荧光屏上观察到亮点,试求粒子在磁场中运动的轨道半径r,并确定磁场区域的半径R应满足的条件.
×105m/s.若能在荧光屏上观察到亮点,试求粒子在磁场中运动的轨道半径r,并确定磁场区域的半径R应满足的条件.
(2)若只在两板间加恒定电压U,M和N相距为d,板长为L(不考虑电场边缘效应).若入射粒子是电量为e、质量为m的电子,它们的速度v满足0< v ≤v0,试求打在荧光屏P上偏离点O2最远的粒子的动能.
(3)若只在两板间加如图乙所示的交变电压u,M和N相距为d,板长为L(不考虑电场边缘效应).入射粒子是电量为e、质量为m的电子.某电子在t0=L/4v0时刻以速度v0射入电场,要使该电子能通过平行金属板,试确定U0应满足的条件.
26.(16分) X、Y、Z、W四种元素原子序数依次增大,X是地壳中含量最高的金属元素,Y原子的最外层电子数是次外层电子数的一半,W元素的原子序数是X元素的两倍。Z单质可发生如下反应:Z
+ OH? 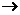 Z2? + ZO32?
+ H2O(未配平),M为Z的最高价氧化物对应的水化物。
Z2? + ZO32?
+ H2O(未配平),M为Z的最高价氧化物对应的水化物。
请回答:
(1)X与M的浓溶液反应必须加热,原因是______________________。
(2)关于Y的有关叙述正确的是(填序号)_______________________。
①Y单质是光导纤维的主要原料②Y的气态氢化物比硫化氢稳定
③Y的最高价氧化物形成的晶体为原子晶体
④Y的最高价氧化物可以和水作用生成相应的酸
(3)工业生产单质X的原理是(用化学方程式表示)____________________。
写出X的最高价氧化物的水化物与NaOH溶液反应的离子方程式____________。
(4)在少量W单质与M的稀溶液反应后的溶液中,加入足量H2O2,反应现象为
_____________,写出反应的离子方程式______________________________。
(5)常温下某单质为液态,96g该单质能与28gW单质恰好完全反应,将所得产物溶
于水配成500mL溶液,求所得溶液中金属离子浓度______________。
27. (14分)下图表示各物质间的转化关系。已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2∶1,常用作干燥剂,D、E为单质。
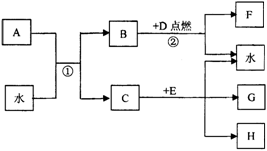
请回答:
(1)写出反应①的化学方程式____________;已知B的燃烧热是1300kJ? mol?1,写出
反应②的热化学方程式______________________。
(2)G和H的混合物俗称__________,在空气中易失效需密封保存,其原因(用化学
方程式表示)___________________________、__________________________.
(3)E和NO2在室温下可以化合生成一种新的气态化合物。实验测知:取E和NO2
混合气体5L,当E所占体积分数分别为20%、60%,反应后气体的体积均为4L(所
有气体体积在相同条件下测得)。生成的气态化合物的分子式_____________反应的化学方程式___________________。
28.(12分)某有机物X(C11H9O6Br)分子中有多种官能团,其结构简式为: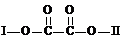
(其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如下转化
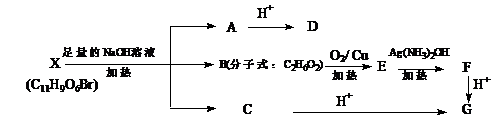
已知向D的水溶液中滴入FeCl3溶液发生显色反应,滴入NaHCO3溶液有无色无味
气体产生,且D苯环上的一氯代物有两种。
(1)D中含氧官能团的名称: ;X的结构简式:
(2)写出B→E的化学方程式:
(3)D不可能发生的反应有:
A.加成反应 B.消去反应 C.取代反应 D.氧化反应 E.加聚反应
(4)D有多种同分异构体,遇FeCl3溶液发生显色反应,又能发生银镜反应,其中能水解的同分异构体的结构简式为: ,其中不能水解的同分异构体的结构简式为: (各写出一种)
29.(18分)某课外活动小组对甲酸(HCOOH)进行了如下的实验,以验证其含有醛基,并考察其化学性质,首先做了银镜反应.
(1)某同学很成功地做了银镜反应,他肯定没有进行的操作________(写字母):
A、用洁净的试管;
B、在浓度为2%的NH3?H2O中滴入稍过量的浓度为2%的硝酸银;
C、用前几天配制好的银氨溶液;
D、在银氨溶液里加入稍过量的甲酸;
E、用小火对试管直接加热;
F、反应过程中,振荡试管使之充分反应.
然后,同学们对甲酸与甲醇进行了酯化反应的研究:
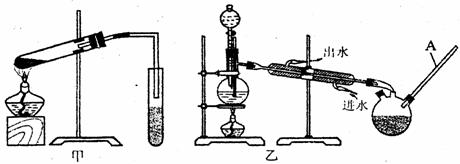 |
(2)乙装置中长导管A的作用是___________________,装在三颈瓶中的是_____________。
(3)写出甲酸和甲醇进行酯化反应的化学方程式______________________.
(4)选择甲装置还是乙装置好?________,主要原因是______________________.
A.甲装置简单,可直接加热反应速率快 B.乙装置使用了温度计可控制反应温度
C.甲醇有毒,需防止(或减少)其逸出。
(5)一同学用装有某溶液的三颈瓶接收甲酸甲酯,收集到的产物很少,请你推测他可能用了什么溶液并结合化学方程式给予合理的解释________________ ______
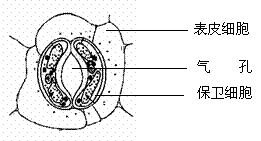
30.(18分)I.(11分)植物的气孔是指叶片表皮中成对的保卫细胞之间的孔隙(见下图)。脱落酸对气孔的开闭具有调节作用, 其作用机理是通过改变保卫细胞中K+的浓度,导致保卫细胞吸水或失水,使气孔开放或关闭。请回答以下问题:
(1)验证K元素属于必需矿质元素常采用的方法是__________________;若除去完全营养液中的K+培养植物,先表现缺素症的是植物_____________(幼嫩、成熟)的叶片。
(2)K元素对光合作用的影响主要通过影响糖类的______________来实现。
(3)夏季晴朗的中午,气孔关闭对______ (C3、C4)植物光合作用的影响更为显著,原因是_____________________________________________________。
 (4)下表为蚕豆保卫细胞中气孔开闭时K+的浓度,请回答以下问题:
(4)下表为蚕豆保卫细胞中气孔开闭时K+的浓度,请回答以下问题:
|
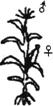 II.(7分)玉米是雌雄同株植物,顶生雄花序,腋生雌花序,如图所示。
II.(7分)玉米是雌雄同株植物,顶生雄花序,腋生雌花序,如图所示。 22、I、(6分)(1)减小α的角度;(2)P3挡住P1P2的像(3)sinβ/sinα
22、I、(6分)(1)减小α的角度;(2)P3挡住P1P2的像(3)sinβ/sinα 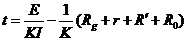 (2分)
(2分)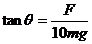 (2分)得
(2分)得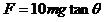 …………(2分)
…………(2分)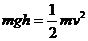 …………(2分)
…………(2分) 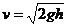 ………………(2分)
………………(2分) 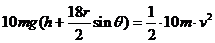 (2分) 得
(2分) 得 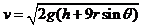 …(2分)
…(2分)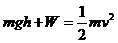 ……(2分)
……(2分)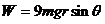 ………(2分)
………(2分) 感应电动势
感应电动势 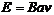 (1分)总电阻
(1分)总电阻 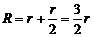 (1分)
(1分)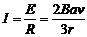 (1分)
(1分)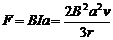 (1分)
(1分)
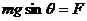 (1分) 联立①-⑤解得:
(1分) 联立①-⑤解得: 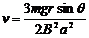 (1分)
(1分)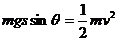 (2分)解得:
(2分)解得: 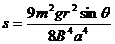 (1分)
(1分)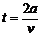 (2分)
(2分)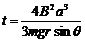 (1分)根据平衡条件
(1分)根据平衡条件 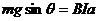
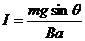 则通过MN边的感应电荷量
则通过MN边的感应电荷量 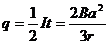 (2分)
(2分)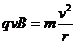 (1分)
(1分)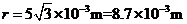 (1分)
(1分) 如图所示,设恰好在荧光屏P上观察到亮点时,粒子偏转角为2θ,磁场区域的最大半径为R0,由几何关系可知
如图所示,设恰好在荧光屏P上观察到亮点时,粒子偏转角为2θ,磁场区域的最大半径为R0,由几何关系可知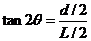 ,
,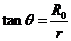 (1分)
(1分)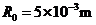 (1分)
(1分)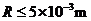 (1分)
(1分)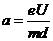 (1分)
(1分)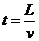
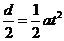 (1分)
(1分)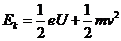 (2分)联列解得
(2分)联列解得 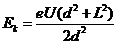 (1分)
(1分)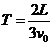 ,则
,则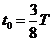 (1分)
(1分)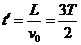 (1分)电子在两极板间的加速度
(1分)电子在两极板间的加速度 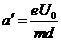 (1分)
(1分)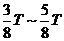 、
、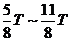 、
、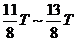 、
、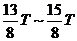 时间内沿垂直于初速度方向运动的位移依次为y1、y2、y3、y4,则有
时间内沿垂直于初速度方向运动的位移依次为y1、y2、y3、y4,则有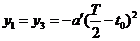 (1分)
(1分)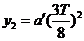 (1分)
(1分)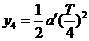 (1分)
(1分)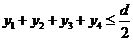 (2分)
(2分)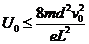 (2分)
(2分)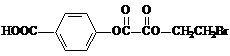 (2分)
(2分) (2)HOCH2―CH2OH+O2
OHC―CHO+2H20
(2分)
(2)HOCH2―CH2OH+O2
OHC―CHO+2H20
(2分) 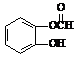
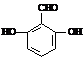 (其他合理答案也可)
(其他合理答案也可)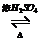 HCOOCH3+H2O
HCOOCH3+H2O