2008年江苏省启东中学中考模拟考试(八)
化学试卷
可能用到的相对原子质量:C―12 H―1 O―16 Cu―
N―14
一、选择题(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.能源的开发和利用关系到社会的进步和发展,有关能源的认识错误的是 ( )
A.化石燃料在地球上的蕴藏量是有限的
B.乙醇汽油的使用可以节省资源,减少汽车尾气的污染
C.使用天然气不会对环境造成任何污染
D.开发新能源可解决能源短缺问题
2.下列符号只有微观意义的是 ( )
A.Cl2 B.2N
3.学习了化学使我们对商品的标签和标识有了更深层次的认识。图8―1中四枚标识使用不
恰当的是 ( )

4.对分子、原子、离子的下列认识中正确的是 ( )
A.氢原子是最小的微粒,不可再分
B.镁原子的质子数大于镁离子的质子数
C.当液态水变成冰,水分子间不存在间隔
D.分子、原子、离子都可以直接构成物质
5.根据物质的用途体现物质的性质这一关系,判断下列说法中错误的是 ( )
A.金刚石可以刻划玻璃,说明金刚石硬度大
B.一氧化碳可用于工业炼铁,说明一氧化碳具有还原性
C.二氧化碳能使紫色石蕊试液变红,说明二氧化碳具有碱性
D.活性炭可用于防毒面具,说明活性炭具有吸附性
6.如图8―2所示,给饱和的澄清石灰水加热,以下叙述中不正确的是 ( )
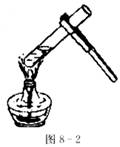
A.氢氧化钙的溶解度随温度的升高而增大
B.溶液由澄清变浑浊
C.溶液仍为饱和溶液
D.溶液中溶质的质量分数减小
7.下列关于铁和铁合金的有关说法错误的是 ( )
A.工业上用一氧化碳将铁矿石中的铁还原出来
B.铁的合金是绝对不会生锈的
C.制造铁轨、船舶、桥梁的碳素钢是铁和碳的合金
D.使用铁锅烧饭菜能为人体提供微量的铁元素
8.漂白粉的主要成分是氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2],因其良好的消毒、漂白和 除臭性能在日常生活中得到广泛的应用。下面关于漂白粉的说法正确的是 ( )
A.氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2]中氯元素的化合价相同
B.氯化钙(CaCl2)属于盐,次氯酸钙[Ca(ClO)2]属于氧化物
C.氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2]都属于盐
D.次氯酸钙[Ca(ClO)2]中含有的原子团ClO的化合价为-2价
9.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的品质。假设用醋酸的质量分数为3%的半成品醋生产
A.
10.下列关于生活中常用材料的认识,正确的是 ( )
A.涤纶、羊毛和棉花都是天然纤维
B.各种塑料在自然界都不能降解
C.电木插座破裂后可以热修补
D.装食品用的聚乙烯塑料袋可以通过加热进行封口
11.用氯化钠固体配制

A.②④⑥⑦ B.①④⑤⑥ C.①③⑤⑦ D.①②④⑦
12.下列化学反应,一般要借助其他试剂才能判断反应发生的是 ( )
A.氯化钾溶液与硝酸银溶液混合 B.碳酸钠溶液与饱和石灰水混合
C.石灰石投入稀盐酸中 D.稀硫酸与氢氧化钠溶液混合
13.下列有关物质用途的说法中,正确的是 ( )
①用稀硫酸清除钢铁表面的铁锈 ②用碳酸氢钠作焙制糕点的发酵粉
③用氢氧化钠中和胃中过多的盐酸 ④用熟石灰中和硫酸工厂的污水
A.①②④ B.①②③ C.②③④ D.①②③④
14.乙烯(C2H4)是石油炼制的重要产物之一。常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是 ( )
A.H2 B.CH
15.小婷同学想用实验证明高锰酸钾溶液的紫红色是MnO4一离子的颜色,而不是K+离子的颜色,他设计的下列实验事实与证明该问题无关的是 ( )
A.将高锰酸钾晶体加热分解,所得固体质量减少
B.观察氯化钾、硝酸钾、硫酸钾溶液都没有颜色,表明溶液中K+离子无色
C.向氯化钾溶液中加入过量锌粉,振荡,静置后未见明显变化,表明锌与K+离子不反应
D.向高锰酸钾溶液中加入过量锌粉,振荡,静置后见紫红色褪去,表明MnO4一离子呈紫红色
二、选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要选错一个,该小题就为0分)
16.下表列出了除去物质中所含少量杂质的方法,其中正确的是 ( )
物质
所含杂质
除去杂质的方法
A
CO气体
CO2
通过足量氢氧化钠溶液,并干燥
B
NaOH溶液
Na2CO3
加入足量稀盐酸至不再产生气泡
C
CaO固体
CaCO3
加水溶解,过滤
D
FeSO4溶液
CuSO4
加入足量锌粒,充分反应,过滤
17.下列认识或说法中正确的是 ( )
A.向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32一
B.常温下可用Fe与AgCl反应制取Ag
C.可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4
D.分别将Mg、Fe、Cu、Ag放入稀盐酸中,可确定它们的活动性顺序
18.同学们在做实验时发现,将镁条放入某CuCl2溶液中,镁条表面有气泡产生。对于这一异常现象产生的原因,同学们设计了以下探究方案进行讨论,其中没有意义的是( )
A.甲同学推测该气体可能是H2,并收集气体用点燃法检验
B.乙同学猜想该CuCl2溶液呈酸性,并用pH试纸检测
C.丙同学用锌粒与该CuCl2溶液反应,观察是否有气泡产生
D.丁同学用镁粉与该CuCl2溶液反应,观察产生气泡的快慢
19.图8―3为M、N两种物质在饱和溶液中溶质的质量分数(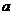 %)随温度(T)变化的曲线,现将
%)随温度(T)变化的曲线,现将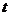 ℃。下列说法正确的是(溶液加热时,M、N不挥发也不发生反应) ( )
℃。下列说法正确的是(溶液加热时,M、N不挥发也不发生反应) ( )
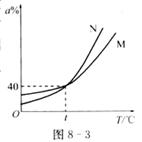
A.M、N都从溶液中析出 B.只有N从溶液中析出
C.M的溶液为饱和溶液 D.N的溶液为饱和溶液
20.某同学利用一黑色粉末(含氧化铜、炭粉、铁粉中的一种或多种)和未知溶质质量分数的稀硫酸,做如下探究:将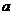 g黑色粉末加入到盛有
g黑色粉末加入到盛有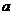 )g。他对实验的推理正确的是 ( )
)g。他对实验的推理正确的是 ( )
A.反应后不可能得到红色固体
B.黑色粉末中含有铁粉,加入黑色粉末质量一定为5.
C.若反应后黑色粉末无剩余,则黑色粉末中一定不含有炭粉
D.该稀硫酸中溶质的质量分数不低于19.6%
三、填空题(本题包括7小题,每空1分,共32分)
21.缺铁性贫血是影响人类健康的一种疾病,诺贝尔奖的获得者费舍尔发现卟啉铁(C34H32ClFeN4O4)对缺铁性贫血有显著疗效。卟啉铁中含有 种元素,1个卟啉铁分子中含有 个碳原子。其实最自然的补铁是食物补铁,含铁丰富的食物有动物肝脏、瘦肉、豆类等,这里的铁指的是 (填铁原子、铁元素、铁分子)。
22.找出物质之间的相互联系和区别,从中发现规律,这是我们学好化学的一种基本方法。下面是五种含氮元素物质的化学式:a.N2;b.NH3;c.N2O4;d.N2O;e.HNO3。
请你回答:
(1)五种物质中氮元素的化合价由低到高的顺序是 (用序号表示)。
(2)仔细观察,在这五种物质中,你还可以发现其他几个规律,请你写出其中两个,并排列成序(排列顺序用序号表示):
① ;② 。
23.图8―4为某品牌燕麦片标签中的一部分:
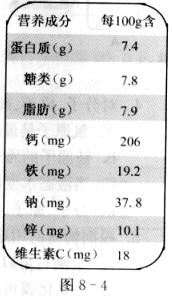
(1)图中出现了六大类营养素之中的 类。
(2)图中出现了 种人体所需的微量元素。
(3)人体健康离不开钙元素,下列有关钙元素的叙述不正确的是(填序号) 。
①人体中钙元素大部分存在骨骼和牙齿中
②幼儿及青少年缺钙会得佝偻病和发育不良
③老年人缺钙会发生骨质疏松,容易骨折
④成年人比幼儿和青少年需要摄入更多的钙
(4)假设每克蛋白质完全氧化放出热量约为18 kJ,则每
24.探究是一种重要的学习方式,是充分理解学科本质的基本途径。在加热氯酸钾和二氧化锰制取氧气的过程中,鉴于制得的氧气有氯气的气味,认为反应过程如下:
①2KclO3+2MnO2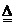
②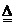 K2MnO4+MnO2+B↑
K2MnO4+MnO2+B↑
③Cl2+K2MnO4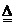 2KCl+MnO2+B↑
2KCl+MnO2+B↑
写出A、B的化学式:A 、B 。
通过以上实例,谈谈你对二氧化锰作催化剂的认识 。
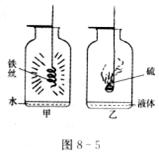
图8―5是同学们在探究氧气性质实验中改进的实验装置图,你认为乙装置中加入的液体是 ;简要回答甲、乙两个集气瓶中液体的作用: 、
。
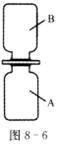
25.在化学晚会上,小林同学表演了一个化学小魔术“空瓶生烟”(如图8―6所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟。请你根据所学知识回答下列问题:
(1)若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图8―7表示为:
”表示氯原子,上述反应过程可用图8―7表示为:
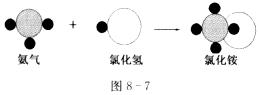
该反应的化学方程式为 。
分析以上微观模拟图,你能得出的结论是 。(写一条)
(2)“烟”是由固体小颗粒形成的,如果这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是 。
(3)生成物氯化铵是一种常见的化肥,它属于化肥中的 肥(填“氮”“磷”或“钾”),此化肥不能与 混合使用。
26.
(1)H2S中硫的化合价为 价。氢硫酸与盐酸一样能与NaOH溶液发生中和反应,生成硫化钠和水。写出该反应的化学方程式: 。
(2)当发生井漏事故时,下列自救措施合理的是 (填序号)。
A.逃生时应往地势高处逆风跑
B.逃生时应往地势低处顺风跑
C.立即用浸过水或弱碱性溶液的毛巾捂住口鼻
(3)为降低危害程度,可以将喷出的气体点燃,其中硫化氢燃烧时,生成二氧化硫和水,该燃烧反应的化学方程式为 ;消防队员还可向空中喷洒 ,以减少空气中硫化氢的含量。
(4)违反操作规程或安全设施不完备,是引发事故的常见原因,请结合具体的化学实验,说出避免实验事故应注意的一个问题: 。
27.X和白色沉淀Ⅰ、Ⅱ都是含有镁元素的化合物,Z是一种会使地球产生“温室效应”的气体,A是一种碱。它们的有关变化如图8―8所示(该实验条件下,微溶物以沉淀形式出现):
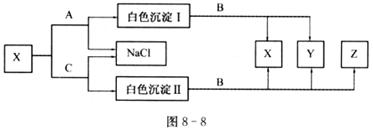
(1)写出下列物质的化学式:A是 ,B是 ,白色沉淀I是 , Z是 。
(2)X跟C反应的化学方程式是 。
四、实验题(本题包括3小题,化学方程式每空2分,其余每空1分,共18分)
28.正确的基本实验操作是确保实验成功和安全的前提。试回答:
(1)量液时,量筒必须放平,视线 。
(2)用漏斗过滤时,注意液面始终要 。
(3)稀释浓硫酸时,切不可将 。
29.
(1)下列除去污水中臭味最有效的方法是 ( )
A.搅拌 B.吸附 C.静置 D.过滤
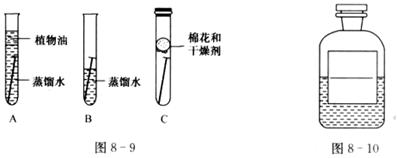
(2)某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图8―9所示。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
①通过探究发现:铁生锈是铁与 和 共同存在时发生化学反应的结果。
②A中加入的蒸馏水要事先煮沸,其目的是 。
(3)某同学配制
30.请参与某学习小组进行研究性学习的过程,并协助完成相关任务:
[提出问题]在平时探讨酸的性质时,我们通常是讨论酸的水溶液。究竟水在酸显示酸的特性时扮演什么角色呢?
[确定研究对象]以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究。
[查阅资料]氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(图8―11)。
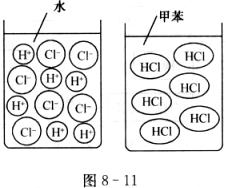
[设计与实验](请完成下表)
实验内容
实验现象
解释与结论
测定导电性
氯化氢的水溶液:导电性良好
氯化氢的水溶液中有自由移动的离子
氯化氢的甲苯溶液:不导电
氯化氢的甲苯溶液没有自由移动的离子
与镁作用
氯化氢的水溶液:①
化学方程式:②
氯化氢的甲苯溶液:没有明显现象
氯化氢的甲苯溶液没有解离出氢离子
与固态碳酸钠作用
氯化氢的水溶液:产生气泡
化学方程式:③
氯化氢的甲苯溶液:④
氯化氢的甲苯溶液没有解离出氢离子
[讨论与反思]盐酸的酸性是因为氯化氢在水分子的作用下解离出了⑤ 。水对酸显现其酸性性质非常重要。还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢?是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注。)
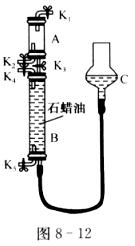
[拓展探究]该学习小组又尝试用图8―12所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好)。通过调节活塞,用排石蜡油的方法在B管中收集满了氨气,如通过调节活塞K1、K2,在干燥的A管中充满与大气压强相等的干燥氯化氢气体,其操作是⑥ 。在不用任何试剂的情况下,当看到现象⑦ 时,说明A管中已收集满了氯化氢气体。打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:⑧ 。
五、计算题(本题包括2小题,共10分)
31.秸秆是一种相对清洁的可再生能源,平均含硫量只有千分之三点八(3.8‰),而煤的平均含硫量约为百分之一(1%)。某地燃烧秸秆的发电厂一年燃烧秸秆约2.0×105t,可节约煤1.0×105t。假设燃料中的硫元素经燃烧后全部转化为SO2,试计算该发电厂燃烧秸秆比燃烧煤每年少排放SO2多少吨?
32.一化学小组为了测定某铜矿中碱式碳酸铜[Cu2(OH)2CO3]的质量分数,称取该铜矿 样品
(1)稀盐酸中HCl的质量是多少克?
(2)铜矿中碱式碳酸铜的质量是多少?其质量分数是多少?
(3)反应后所得氯化铜溶液中溶质的质量分数是多少?
(反应的化学方程式为:Cu2(OH)2CO3+4HCl==2CuCl2+CO2↑+3H2O。
反应中各物质的相对分子质量:Cu2(OH)2CO3―222 HCl―36.5 CuCl2―135
CO2―44 H2O―18)