网址:http://m.1010jiajiao.com/timu_id_904793[举报]
某校化学兴趣小组的同学利用下列装置进行实验。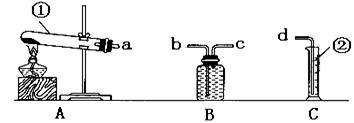
实验目的:
一.用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
二.粗略测定加热2g高锰酸钾所收集到的氧气体积。
反应原理:(用化学式表达式表示)
高锰酸钾制氧气: 。
细铁丝在氧气中燃烧: 。
装置连接:
写出标数字的仪器名称:① ,② 。
为达到实验二的目的,各装置的正确连接顺序是:(填接口的字母)a→ → →d。
问题分析:
(1)实验过程发现B瓶中的水变红了,原因是: 。
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是: 。
(3)在本实验中,收集氧气的时机是加热后马上收集,若是在气体连续不断产生之后才开始收集,则测得的氧气的体积会比实际值 (填“偏大”或“偏小”或“不变”)。
(4)实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰装入试管,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变.则猜想 错误。
②第二组同学取锰酸钾装入试管,在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 。
某校化学兴趣小组的同学准备对某生铁样品中铁的含量进行探究。请你按要求帮助他们完成下列探究报告。
[提出问题]生铁是纯铁吗?若不是纯铁则该生铁样品中铁单质的质量分数是多少?
[查阅资料] ⑴生铁中除铁外,还含有碳、硅、锰等元素。
⑵碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰等存在形式较为复杂。
⑶含有硅、锰等元素的物质通常都不与稀硫酸发生化学反应。
[制定方案]使生铁样品与过量的稀硫酸反应,称量反应前后物质的质量差。
[实验过程]
⑴取一只烧杯,称得其质量为70.4 g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4 g;
⑵向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入稀硫酸以确保过量,测得共用去稀硫酸247.3 g;
⑶静置,称量。称得烧杯和剩余物质的总质量为348.7 g。
[数据处理]通过对以上数据的分析和计算,该生铁样品中铁单质的质量分数为 %。
[交流讨论]
⑴实验称量时称量物应放在托盘天平的 盘(选填“左”或“右”)。
⑵实验过程中稀硫酸要过量的原因是 。
⑶反应过程中可看到有气泡冒出,溶液由无色变为浅绿色,由此得知反应一定生成了氢气和 (写名称)。
⑷经质检部门精确测定,该样品中铁元素的总质量分数为95.2%。对此有同学产生了疑问,请你帮他分析: 。
[实验结论]经过以上探究,同学们知道了生铁不是纯铁,实际上它属于铁的重要 。
查看习题详情和答案>>某校化学兴趣小组的同学利用下列装置进行实验。

实验目的:
一.用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
二.粗略测定加热2g高锰酸钾所收集到的氧气体积。
反应原理:(用化学式表达式表示)
高锰酸钾制氧气: 。
细铁丝在氧气中燃烧: 。
装置连接:
写出标数字的仪器名称:① ,② 。
为达到实验二的目的,各装置的正确连接顺序是:(填接口的字母)a→ → →d。
问题分析:
(1)实验过程发现B瓶中的水变红了,原因是: 。
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是: 。
(3)在本实验中,收集氧气的时机是加热后马上收集,若是在气体连续不断产生之后才开始收集,则测得的氧气的体积会比实际值 (填“偏大”或“偏小”或“不变”)。
(4)实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰装入试管,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变.则猜想 错误。
②第二组同学取锰酸钾装入试管,在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 。
查看习题详情和答案>>
【小组讨论】观点Ⅰ:纯碱样品中只含有碳酸钠
观点Ⅱ:纯碱样品是由碳酸钠和少量氯化钠组成的混合物
【实验设计】
甲方案
Ⅰ 设计思路:根据样品与石灰水反应生成沉淀碳酸钙的质量,求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
Ⅱ 操作步骤:称取13.25g纯碱样品,加入过量的澄清石灰水,充分搅拌。过滤、洗涤、干燥,得到白色沉淀10.00g
Ⅲ 数据处理:请根据上述实验数据,计算该样品中碳酸钠的质量分数。
计算过程:______________________________________________________。
Ⅳ 实验结论:____________________________________。
乙方案
Ⅰ 设计思路:根据样品(质量为ag)与稀硫酸完全反应生成二氧化碳的质量(质量为bg),求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。 Ⅱ 实验结论: (1)当a、b的质量关系满足___________________(填写含a、b字母的表达式,下同)时,纯碱样品中只含有碳酸钠,样品中碳酸钠的质量分数是100﹪。
(2)当a、b的质量关系满足___________时,纯碱样品是由碳酸钠和少量氯化钠组成的混合物,样品中碳酸钠的质量分数是_____________。
【实验评价】误差分析:
(1)甲方案中,白色沉淀的质量在过滤、干燥等操作过程中会有所损耗,造成计算结果与实际值相比偏小。
(2)乙方案中,有部分生成的二氧化碳气体因溶解于水而没有全部逸出,造成计算结果与实际值相比____________(填写“偏大”、 “偏小”或“不变”)。
【交流反思】 (1)实验过程中,需用玻璃棒不断搅拌,该操作的目的是________________________。
(2)甲方案实验操作中,对沉淀洗涤的目的是:__________________________。
(3)乙方案中,需用一定质量的19.6﹪的稀硫酸。现有一瓶98﹪的浓硫酸(密度为1.84g/cm3),配制乙方案中实验所用稀硫酸,至少需要浓硫酸的体积是_________mL(填写含字母的表达式)。浓硫酸稀释的正确操作是______________________。