2006-2007学年度淄博市沂源县第二学期期末考试
初三化学试题
可能用到的相对原子质量:H l C l2 N 14 O 16 Na
一.单项选择题(每个小题3分,共51分;)
1.我们每时每刻都离不开空气,空气成分的微小变化都会直接影响人类的生存,你关注每天的空气质量报告吗?在空气质量报告中一般不涉及
A.二氧化硫 B.二氧化碳 C.氮氧化合物(NO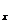 ) D.可吸入颗粒物(TSP)
) D.可吸入颗粒物(TSP)
2.下列物质中,作为燃料时对空气无污染的是
A.煤 B.汽油 C.氢气 D.柴油
3.下列各物质的化学式中氯元素的化合价最高的是
A.Cl2 B.HCIO C.KCl D.KClO3
4.市场上有一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动罐头使它们混合,罐内饮料温度就会降低(俗称“摇摇冰”),则固体物质为
A.氢氧化钠 B.硝酸铵 C.食盐 D.蔗糖
5.我们每天都要喝水,都要用水,水是生命之源,是最常见的溶剂,其化学式为“H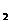 O”。如图所示,下列四位同学正在讨论化学式“H
O”。如图所示,下列四位同学正在讨论化学式“H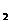 O”的表示意义,其中错误的是
O”的表示意义,其中错误的是

6.下列是家庭常用的调味品 ①食盐 ②味精 ③白糖 ④食用油 ⑤食醋 ⑥酱油,分别放入水中能形成溶液的是
A.只有①③⑤ B.只有①②③⑤ C.只有②④⑥ D.①②③④⑤⑥
7.某物质溶解在水中,形成的溶液与水相比较,一定不会改变的是
A.凝固点 B.导电性 C.颜色 D.水分子结构
8.2008年奥运会将在中国举行,国际奥委会禁止运动员服用兴奋剂。可卡因是一种兴奋剂,其化学式为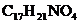 。下列有关卡可因说错误的是
。下列有关卡可因说错误的是
A.可卡因是一种氧化物
B.可卡因由碳、氢、氧、氮四种元素组成的
C.可卡因分子中C、H、O、N的原子个数之比为l7:21:4:l
D.可卡因的相对分子质量的计算式为12×17+1×21+14×1+16×4
9.某氧化物中,含氧元素的质量分数为50%,已知该氧化物的每个分子中含有两个氧原子,该氧化物的相对分子质量为
A.32
B.
10.下列化学方程式书写正确的是
A.氧化汞加热分解: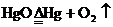
B.铁在氧气中燃烧:
C.锌片投入稀硫酸中: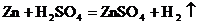
D.碳在氧气中不充分燃烧:
11.在化学反应前后,一定不会变化的是
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤分子的种类 ⑥物质的体积 ⑦物质的状态 ⑧元素的化合价
A.②④⑤ B.①③④ C.①③⑦⑧ D.①③④⑥
12.下列配制一定溶质质量分数的氯化钠溶液的实验操作失误(其它操作都正确),会引起溶质质量分数升高的是
A.用托盘天平称量氯化钠质量时,指针偏右就取下食盐
B.用量筒量取水时,面对刻度线仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,有水溅出
D.将配好的溶液转移到细口瓶时,不慎洒落
13.下列有关燃烧或灭火的说法不正确的是
A.厨房炒菜,油锅不慎着火,立即盖上锅盖,其目的是隔绝油与空气的接触
B.家庭用的煤通常要加工成蜂窝煤,目的是增大氧气的浓度,促进煤燃烧
C.敞口放置在实验室中的酒精没有燃烧的原因是没有达到酒精的着火点
D.室内着火被困,立即用湿毛巾堵住口鼻,匍匐前进,寻找安全口。
14.人们在工作.生活中,为了防止事故的发生,常采取一些安全措施。下列措施安全的是 A.到溶洞里探险用火把照明
B.在密封较好的室内生煤炉取暖时,在煤炉附近放一盆清水
C.点燃木条检查液化石油气是否泄漏
D.掏空沼气池前进行灯火试验
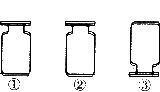
15.右下图是老师放置在实验桌上的三瓶无色气体,它们可能是H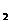 、O
、O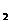 、CO
、CO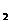 。下列关于这三种气体的鉴别方法中,不正确的是
。下列关于这三种气体的鉴别方法中,不正确的是
A.根据③倒置,可判断③存放的是H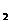 。
。
B.用带火星的木条放入①中,若复燃,则存放的是O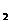
C.用点燃的木条伸入②中,若火焰熄灭,则存放的是CO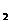
D.向②中加入少量蒸馏水,若变为红色,则存放的是CO
16.点燃某可燃物后,在火焰上方罩一冷而干燥的烧杯,烧杯内壁有水出现,把烧杯迅速倒过来,立即向烧杯内注入少量澄清石灰水,振荡,石灰水变浑浊,该气体可能是
A.CH B.H
B.H C.C
D.O
C.C
D.O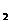
17.在反应
A.4:19 B.3:
二.理解与应用(本题包括3个题,共21分)
18.(5分)按下列要求填写空白:
(1)空气中含量最多的气体的化学式: ;
(2)氧化铜的化学式: ;(3)两个三氧化硫分子: ;
(4)标出CH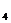 中碳元素的化合价: ;(5)一个钠离子:
。
中碳元素的化合价: ;(5)一个钠离子:
。
19.(12分)按下列要求写出化学方程式:
(1)有水生成的氧化反应: ;
(2)有水参加反应的化合反应: ;
(3)有水生成的分解反应:① ,② ;
(4)有水参加反应的分解反应: ;
(5)有水生成,但此反应既不是化合反应,也不是分解反应: 。20.(4分)依据联合国《京都议定书》公约,要求限制二氧化硫.二氧化碳等气体排放量,以控制日趋严重的环境污染,保护人类居住的地球。
(1)如果大气中二氧化碳等气体的含量过高,会引起全球气候变暖,这种现象称为 效应。
(2)为减少大气中二氧化碳的含量,你建议采取的可行措施① ;② 。
(3)为解决全球变暖的难题,进年来科学家采取了许多措施,其中用到“组合转化”技术:将二氧化碳和氢气以一定比例混合,在一定条件下反应,生成一种重要的化工原料乙烯(C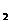 H
H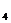 )和一种常见的物质,其反应的化学方程式为
)和一种常见的物质,其反应的化学方程式为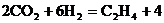 。
。
三.实验与探究((本题包括5个题,共29分)
21.(5分)配制l
22.(2分)右图是铁在氧气燃烧的实验装置图,集气瓶中加入水的作用是 ;铁丝绕成螺旋状的目的是 。

23.(4分)早在17世纪,质量守恒定律被发现之前,英国化学家波义耳曾做过一个实验:在密闭的玻璃容器中燃烧金属时,得到了金属灰,然后称量金属灰的质量,发现比原金属质量增加了。该实验导致波义耳与质量守恒定律擦肩而过。
(1)试解释金属灰质量比原金属质量增加的原因。
。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
。
24.(11分)某学校化学实验小组探究二氧化碳的制取及其性质,所用的实验装置如下:
问题:
(1)写出图中所标仪器的名称:a ;b ;c 。
(2)用装置A制取二氧化碳,所用药品为 (写药品的名称)。
(3)B处观察到的现象是 。
(4)若用装置C证明二氧化碳与水反应,装置C中可盛放的试剂是 ,现象是 。
(5)实验装置E中,可观察到镁条在二氧化碳气体中剧烈燃烧,发出白光,产生一种白色粉末和一种黑色粉末。写出该反应的化学方程式 。通过实验E,还可以引发你对过去某些知识(燃烧和灭火)的反思,从而有些新的发现:①
,②
。
25.(7分)为了制取少量的氧气,化学兴趣小组的同学把工作分为以下三个阶段:
Ⅰ查阅资料,获得信息:过氧化氢、氯酸钾、高锰酸钾等含有氧元素的物质在一定条件下分解都可以产生氧气,其中过氧化氢价格最低,在常温下就能够分解放出氧气,该过程无副产物;氯酸钾价格较高,分解较困难,且常伴有副产物;高锰酸钾价格较高,加热即可快速分解。二氧化锰能加速上述三种物质的分解。
根据上述信息,确定制取氧气的实验方案。
Ⅱ组装仪器,进行实验。可供选择的实验装置如下:

(1)要制取一瓶氧气,你认为应选择的最佳实验装置是 (填写字母代号);组装好实验装置后首先应 ;实验完毕后,欲分离混合物中的二氧化锰应采用的实验操作是 。
(2)有气体产生的化学反应在有限的空间里发生时,如果反应速度过快,容易引起爆炸。在用纯过氧化氢和二氧化锰制氧气的实验中,为预防爆炸应采取的措施 .
(列举两条)。
(3)回顾整个工作过程,你认为在准备工作阶段除应考虑药品的价格.制氧气反应的难易.制氧气过程的安全性等因素外,还应考虑的因素是 .
(列举两条)。
四.分析与计算(本题包括3个题,共l9分)
26.(4分)味精的主要成分为谷氨酸钠(化学式为 Na),因能增加食品的鲜味、促进食欲而成为家庭常用的调味品。试计算:
Na),因能增加食品的鲜味、促进食欲而成为家庭常用的调味品。试计算:
(1)谷氨酸钠的相对分子质量是 ;
(2)谷氨酸钠中氮元素的质量分数是 (精确到0.1%)。
化学式:HCI 相对分子质量:36.5
密度: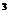 质量分数:36%
质量分数:36%
欲配制l
28.(10分)某学校的化学兴趣小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法是;取该石灰石样品
实验次数
加入稀盐酸的质量/g
剩余固体的质量/g
1
5
1.5
2
5
1.0
3
5
0.3
4
5
n
根据实验数据计算:
(1)表中n的数值为 。
(2)样品中碳酸钙的质量分数是 。
(3)求盐酸中溶质的质量分数。