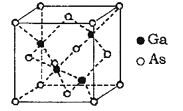
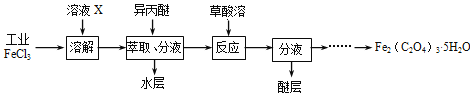
【题目】为证明过氧化钠可在呼吸面具和潜水艇中作为氧气的来源,某化学兴趣小组选择适当的化学试剂和实验用品,用如图所示的装置(C中盛放的是过氧化钠)进行实验。回答下列问题:

(1)a的名称______。
(2)A是实验室中制取CO2的装置。写出A中发生反应的离子方程式:______。
(3)填写如表中的空白。
装置序号 | 加入的试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | ____ |
D | ____ | ____ |
(4)写出C中发生反应的化学方程式:______。
(5)F中得到气体的检验方法______。
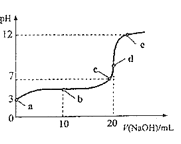
(6)为了测定某碳酸钠样品的纯度,完成如下实验:在电子天平上准确称取三份灼烧至恒重的无水Na2CO3样品(杂质不与盐酸反应)0.4000g于250mL锥形瓶中,用50mL水溶解后,加2~3滴______作指示剂,然后用0.2000molL-1HCl标准液滴定,滴定终点的实验现象为______。已知:Na2CO3与HCl的滴定反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,滴定时实验数据列表如表:
实验次数编号 | 0.2000molL-1HCl溶液的体积(mL) | |
滴定前刻度 | 滴定后刻度 | |
1 | 1.00 | 31.50 |
2 | 5.00 | 34.50 |
3 | 7.00 | 42.50 |
选取上述合理数据,计算出碳酸钠样品的纯度为______。
【题目】中科院大连化学物理研究所的一项最新成果实现了甲烷高效生产乙烯。甲烷在催化作用下脱氢,在不同温度下分别形成CH3、![]() 等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)。
等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)。
物质 | 燃烧热(kJmol-1) |
氢气 | 285.8 |
甲烷 | 890.3 |
乙烯 | 1411.0 |
(1)已知相关物质的燃烧热如表所示,写出甲烷制备乙烯的热化学方程式______。
(2)现代石油化工采用Ag作催化剂,可实现乙烯与氧气制备X(分子式为C2H4O,不含双键)。该反应符合最理想的原子经济,则反应产物是______(填结构简式)。
(3)在一定条件下,向2L的恒容密闭反应器中充入1molCH4,发生上述(1)反应,10分钟后达到平衡,测得平衡混合气体中C2H4的体积分数为20.0%.则:
①用CH4表示该反应的平均速率为______。
②在该温度下,其平衡常数K=______。
③下列说法正确的是______。
a.升高温度有利于提高C2H4的产率
b.向平衡体系中充入少量He,CH4的转化率降低
c.当混合气体的密度不再变化时,说明该反应达到平衡状态
d.向上述平衡体系中再充入1molCH4,达到平衡后H2的体积分数减小
e.若实验测得:v(正)=k(正)c2(CH4),v(逆)=k(逆)c2(H2)c(C2H4)。其中k(正)、k(逆)为受温度影响的速率常数,该反应的平衡常数K=![]()
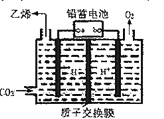
(4)以铅蓄电池为电源,将CO2转化为乙烯的装置如图所示,电解所用电极材料均为惰性电极。电解过程中,阳极区溶液中c(H+)逐渐______(填“增大”、“减小”或“不变”),阴极反应式______。
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数