题目内容
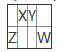
【题目】为证明过氧化钠可在呼吸面具和潜水艇中作为氧气的来源,某化学兴趣小组选择适当的化学试剂和实验用品,用如图所示的装置(C中盛放的是过氧化钠)进行实验。回答下列问题:

(1)a的名称______。
(2)A是实验室中制取CO2的装置。写出A中发生反应的离子方程式:______。
(3)填写如表中的空白。
装置序号 | 加入的试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | ____ |
D | ____ | ____ |
(4)写出C中发生反应的化学方程式:______。
(5)F中得到气体的检验方法______。
(6)为了测定某碳酸钠样品的纯度,完成如下实验:在电子天平上准确称取三份灼烧至恒重的无水Na2CO3样品(杂质不与盐酸反应)0.4000g于250mL锥形瓶中,用50mL水溶解后,加2~3滴______作指示剂,然后用0.2000molL-1HCl标准液滴定,滴定终点的实验现象为______。已知:Na2CO3与HCl的滴定反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,滴定时实验数据列表如表:
实验次数编号 | 0.2000molL-1HCl溶液的体积(mL) | |
滴定前刻度 | 滴定后刻度 | |
1 | 1.00 | 31.50 |
2 | 5.00 | 34.50 |
3 | 7.00 | 42.50 |
选取上述合理数据,计算出碳酸钠样品的纯度为______。
【答案】分液漏斗 CaCO3+2H+=Ca2++H2O+CO2↑ 除去CO2气体中混入的HCl NaOH溶液 吸收未反应的CO2气体 2Na2O2+2CO2=2Na2CO3+O2↑、2Na2O2+2H2O=4NaOH+O2↑ 将带火星的木条伸入瓶中,若木条复燃证明O2 甲基橙 溶液由黄色变为橙色,且半分钟之内无变化 79.5%
【解析】
A中CaCO3+2HCl=CaCl2+H2O+CO2↑,制备CO2,B中装有饱和NaHCO3溶液除去CO2中少量HCl,C中盛放的是过氧化钠,发生反应2Na2O2+2CO2=2Na2CO3+O2↑、2Na2O2+2H2O=4NaOH+O2↑,D中放NaOH溶液,吸收未反应的CO2气体,E收集生成的O2。
(1)a的名称分液漏斗,故答案为:分液漏斗;
(2)A是实验室中制取CO2,化学反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,离子反应方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(3)
装置序号 | 加入的试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
D | NaOH溶液 | 吸收未反应的CO2气体 |
故答案为:除去CO2气体中混入的HCl;NaOH溶液;吸收未反应的CO2气体;
(4)C中盛放的是过氧化钠,发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑、2Na2O2+2H2O=4NaOH+O2↑,故答案为:Na2O2+2CO2=2Na2CO3+O2↑、2Na2O2+2H2O=4NaOH+O2↑;
(5)F中得到气体为氧气,其检验方法:将带火星的木条伸入瓶中,若木条复燃证明O2,
故答案为:将带火星的木条伸入瓶中,若木条复燃证明O2;
(6)盐酸滴定碳酸钠,碳酸钠显碱性,可用甲基橙作指示剂,已知:Na2CO3与HCl的滴定反应为Na2CO3+2HCl═2NaCl+H2O+CO2↑,滴定终点的实验现象溶液由黄色变为橙色,且半分钟之内无变化,由实验数据分析可知,实验次数编号为3的实验误差大,不可用,由1、2平均可得,消耗的盐酸体积为30.0mL,由反应方程式可知,Na2CO3∽2HCl,碳酸钠的物质的量为:n(Na2CO3)=1/2n(HCl)=1/2×0.2000molL×0.03L=0.003mol,m(Na2CO3)= 0.003mol×106g·mol-1=0.318g,碳酸钠样品的纯度为![]() ×100%=79.5%,故答案为:甲基橙;溶液由黄色变为橙色,且半分钟之内无变化;79.5%;
×100%=79.5%,故答案为:甲基橙;溶液由黄色变为橙色,且半分钟之内无变化;79.5%;