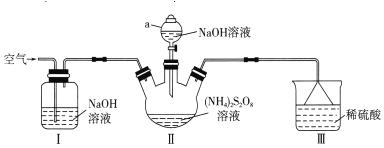
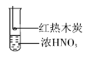
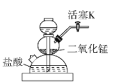
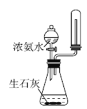
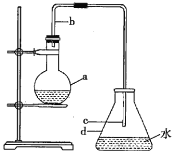
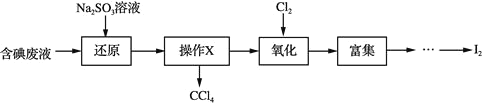
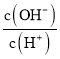0 200762 200770 200776 200780 200786 200788 200792 200798 200800 200806 200812 200816 200818 200822 200828 200830 200836 200840 200842 200846 200848 200852 200854 200856 200857 200858 200860 200861 200862 200864 200866 200870 200872 200876 200878 200882 200888 200890 200896 200900 200902 200906 200912 200918 200920 200926 200930 200932 200938 200942 200948 200956 203614