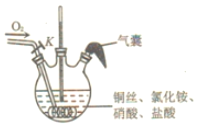
题目内容
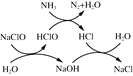
【题目】实验室从含碘废液![]() 除
除![]() 外,含有
外,含有![]() 、
、![]() 、
、![]() 等
等![]() 中回收碘,其实验过程如下:
中回收碘,其实验过程如下:
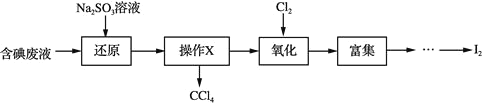
下列叙述不正确的是
A.“还原”步骤发生的反应为:![]()
![]()
B.“操作X”为静置、分液,所得![]() 可用作“富集”的萃取剂
可用作“富集”的萃取剂
C.“氧化”过程中,为使![]() 完全被氧化,需长时间通入
完全被氧化,需长时间通入![]()
D.“富集”即![]() 富集于有机溶剂,同时除去某些杂质离子
富集于有机溶剂,同时除去某些杂质离子
【答案】C
【解析】
A.“还原”的目的是把溶于![]() 的
的![]() 还原为
还原为![]() 而进入水层,反应的离子方程式为:
而进入水层,反应的离子方程式为:![]()
![]() ,故A正确;
,故A正确;
B.把水溶液与有机层![]() 分离,应进行静置、分液,“富集”过程需萃取碘水中的
分离,应进行静置、分液,“富集”过程需萃取碘水中的![]() ,可用
,可用![]() 作萃取剂,故B正确;
作萃取剂,故B正确;
C.“氧化”的目的是把水溶液中的![]() 氧化为
氧化为![]() ,反应的离子方程式为:
,反应的离子方程式为:![]() ,若长时间通入
,若长时间通入![]() ,过量的
,过量的![]() 能氧化
能氧化![]() ,反应的离子方程式为:
,反应的离子方程式为:![]() ,故C错误;
,故C错误;
D.“富集”的目的是利用有机溶剂萃取碘水中的![]() ,以增大
,以增大![]() 的浓度,也可以除去前面“还原”和“氧化”步骤中产生的
的浓度,也可以除去前面“还原”和“氧化”步骤中产生的![]() ,故D正确;
,故D正确;
故选C。

练习册系列答案
相关题目