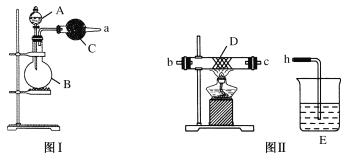
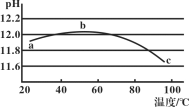
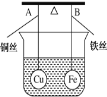
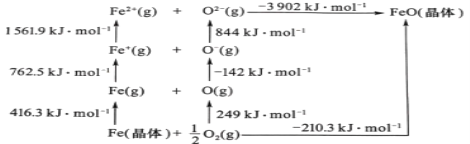【题目】某同学进行如下实验![]() 溶液的浓度均为
溶液的浓度均为![]() 。
。
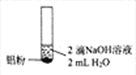
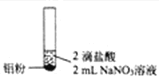
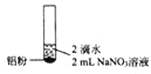
编号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 产生无色气泡 | 产生无色气泡液面上方呈浅红棕色 | 产生无色气泡 |
下列对实验现象的解释或推测不合理的是
A.![]() 中:
中:![]()
B.根据上述实验判断,![]() 的氧化性强于水
的氧化性强于水
C.![]() 中:
中:![]()
D.![]() 中使湿润pH试纸变蓝的气体是
中使湿润pH试纸变蓝的气体是![]()
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | e | f | 83.0 |
①b<f ②915℃、2.0MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A.4个B.3个C.2个D.1个