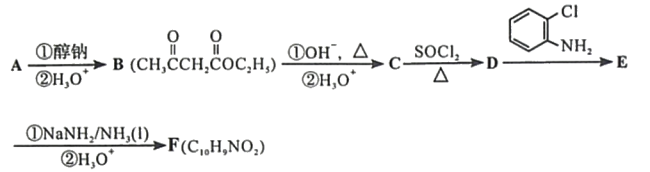
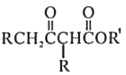
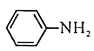
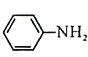
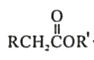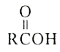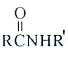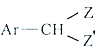0 199133 199141 199147 199151 199157 199159 199163 199169 199171 199177 199183 199187 199189 199193 199199 199201 199207 199211 199213 199217 199219 199223 199225 199227 199228 199229 199231 199232 199233 199235 199237 199241 199243 199247 199249 199253 199259 199261 199267 199271 199273 199277 199283 199289 199291 199297 199301 199303 199309 199313 199319 199327 203614