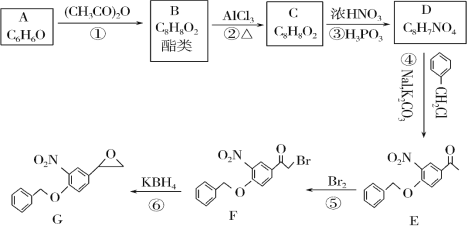
【题目】实验室可用苯乙酮间接电氧化法合成苯甲酸,原理如图所示:
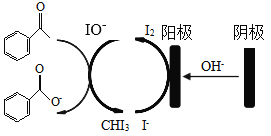
实验步骤如下:
步骤I:电合成:在电解池中加入KI、20mL蒸馏水和20mL的1,4-二氧六环,搅拌至完全溶解,再加入20mL苯乙酮,连接电化学装置,恒定电压下电解7h;
步骤II:清洗分离:反应停止后,将反应液转移至烧瓶,蒸馏除去反应溶剂;用蒸馏水和二氯甲烷洗涤烧瓶,将洗涤液转移至分液漏斗;用二氯甲烷萃取除去质,分离出水相和有机相;
步骤III:制得产品:用浓盐酸酸化水相至pH为1~2,接着加入饱和NaHSO3溶液,振荡、抽滤、干燥,称量得到产品7.8g;
有关物质的数据如下表所示:
物质 | 分子式 | 溶解性 | 沸点(℃) | 密度(g/cm3) | 相对分子质量 |
苯乙酮 | C8H8O | 难溶于水 | 202.3 | 1.03 | 120 |
苯甲酸 | C7H6O2 | 微溶于水 | 249 | 1.27 | 122 |
二氯甲烷 | CH2Cl2 | 不溶于水 | 40 | 1.33 | 85 |
回答下列问题:
(1)步骤I中,阴极的电极反应式为________________________ ,苯乙酮被氧化的离子方程式为_____________________
(2)步骤II蒸馏过程中,需要使用到的玻璃仪器有____________,(填标号)除此之外还需要____________________
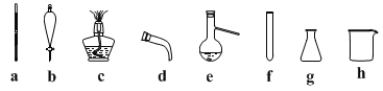
(3)步骤II分液过程中,应充分振荡,静置分层后________(填标号)
A.直接将有机相从分液漏斗的上口倒出
B.直接将有机相从分液漏斗的下口放出
C.先将有机相从分液漏斗的下口放出,再将水相从下口放出
D.先将有机相从分液漏斗的下口放出,再将水相从上口倒出
(4)步骤III中,加入浓盐酸的目的是____________________
(5)步骤III中,加入饱和NaHSO3溶液,水相中的颜色明显变浅,说明过量的I2被还原为I-,其离子方程式为_______________________
(6)本实验的产率是______________(保留小数后一位有效数字)
(7)得到的粗苯甲酸可用____________法进行提纯。
【题目】汽车发动机工作时会产生包括CO、NOx等多种污染气体,如何处理这些气体,对保护大气环境意义重大,回答下列问题:
(1)已知:2NO2(g) ![]() 2NO(g)+O2(g) ΔH1=+115.2 kJ·mol-1;
2NO(g)+O2(g) ΔH1=+115.2 kJ·mol-1;
2O3(g) ![]() 3O2(g) ΔH2=-286.6 kJ·mol-1。
3O2(g) ΔH2=-286.6 kJ·mol-1。
写出臭氧与NO作用产生NO2和O2的热化学方程式:___________。恒容密闭体系中NO氧化率随![]() 值的变化以及随温度的变化曲线如图所示。NO氧化率随
值的变化以及随温度的变化曲线如图所示。NO氧化率随![]() 值增大而增大的主要原因是________________________。
值增大而增大的主要原因是________________________。
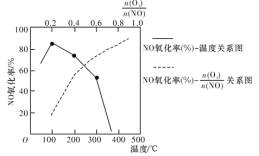
(2)实验测得反应2NO(g)+O2(g) ![]() 2NO2(g) △H<0的即时反应速率满足以下关系式:v正=k正·c2(NO)·c(O2);v逆=k逆·c2(NO2),k正、k逆为速率常数,受温度影响
2NO2(g) △H<0的即时反应速率满足以下关系式:v正=k正·c2(NO)·c(O2);v逆=k逆·c2(NO2),k正、k逆为速率常数,受温度影响
①温度为T1时,在1L的恒容密闭容器中,投入0.6 molNO和0.3 molO2达到平衡时O2为0.2 mol;温度为T2时,该反应存在k正=k逆,则T1_______ T2 (填“大于”、“小于”或“等于”)。
②研究发现该反应按如下步骤进行:
第一步:NO+NO![]() N2O2 快速平衡 第二步:N2O2 +O2
N2O2 快速平衡 第二步:N2O2 +O2![]() 2NO2 慢反应
2NO2 慢反应
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v1正=k1正×c2(NO);v1逆=k1逆×c(N2O2)
下列叙述正确的是______
A.同一温度下,平衡时第一步反应的![]() 越大反应正向程度越大
越大反应正向程度越大
B.第二步反应速率低,因而转化率也低
C.第二步的活化能比第一步的活化能低
D.整个反应的速率由第二步反应速率决定
(3)科学家研究出了一种高效催化剂,可以将CO和NO2两者转化为无污染气体,反应方程式为:2NO2(g)+4CO(g) ![]() 4CO2(g)+N2(g) △H<0
4CO2(g)+N2(g) △H<0
某温度下,向10L密闭容器中分别充入0.1molNO2和0.2 molCO,发生上述反应,随着反应的进行,容器内的压强变化如下表所示:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
压强/kPa | 75 | 73.4 | 71.95 | 70.7 | 69.7 | 68.75 | 68.75 |
回答下列问题:
①在此温度下,反应的平衡常数Kp=_________kPa-1(Kp为以分压表示的平衡常数,计算结果精确到小数点后2位);若保持温度不变,再将CO、CO2气体浓度分别增加一倍,则平衡_____(填“右移”或“左移”或“不移动”);
②若将温度降低,再次平衡后,与原平衡相比体系压强(p总)如何变化?_______(填“增大”、“减小”或“不变”),原因是_____________________。