4.下列有关颜色变化错误的是( )
| A. | 在4mL0.1mol/L的K2Cr2O7溶液中滴加数滴1mol/LNaOH溶液,溶液颜色从橙色变成黄色 | |
| B. | 向血红色的Fe(SCN)3溶液中加入少量KI固体,溶液颜色变浅 | |
| C. | 在试管中加入少量氯化钴晶体,滴加浓盐酸溶解后加水稀释至紫色,将试管置于热水中片刻,溶液颜色变成粉红色 | |
| D. | 用50mL针筒抽取30mL红棕色的NO2气体并封住注射孔,当用力推压活塞,压缩针筒中的气体(此过程中不考虑温度变化),从针筒顶端观察,气体颜色逐渐变浅 |
3.下列说法正确的是( )
| A. | 向Na2S2O3稀溶液中加入稀硫酸,发生如下反应:S2O32-+2H+=SO2↑+S↓+H2O,利用产生浑浊的快慢或产生气泡的快慢可以测定该反应在不同条件下的反应速率 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| D. | 往装有铁钉的试管中加入2 mL水、3滴稀醋酸和1滴K3[Fe(CN)6]溶液,可以观察到铁钉表面粘附气泡,同时周围出现蓝色沉淀,这说明铁钉发生了吸氧腐蚀 |
2.下列叙述中,正确的是( )
| A. | 太阳能、氢能、风能、生物质能都属于新能源 | |
| B. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 | |
| C. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 | |
| D. | 镀层破损后,马口铁比白铁更耐腐蚀 |
1.下列变化过程,属于放热过程的是( )
| A. | 合成氨反应 | B. | 液态水变成水蒸气 | ||
| C. | 弱酸弱碱的电离 | D. | 灼热的炭与CO2的反应 |
20.已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,3Cl2+6NaOH=5NaCl+NaClO3+3H2O.某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液.经测定ClO-与ClO3-的物质的量之比为1:3,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
| A. | 21:5 | B. | 11:3 | C. | 3:1 | D. | 4:1 |
18.下列图示与对应的叙述相符的是( )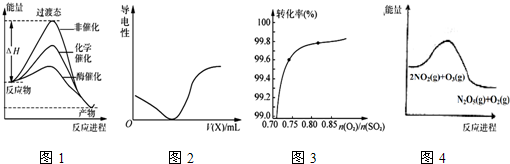

| A. | 由图1所示曲线可知,化学催化比酶催化的效果好 | |
| B. | 在H2S溶液导电性实验中,由图2所示曲线可确定通入的气体X为Cl2 | |
| C. | 其它条件不变,关于反应2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g),图3中纵坐标表示O2的转化率 | |
| D. | 图4的反应升高温度,平衡常数减小 |
17.某温度下,容积同为2L的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知某温度下2HI(g)?H2(g)+I2(g)△H=+AkJ•mol-1 K=4.0)
(1)根据上表回答问题
①c1、c3的关系式为2c1=c3
②a、b的关系式为a+b=A
③p2、p3的关系式为2p2=p3
④a1与a2的关系式为α1+α2=1
(2)甲容器中:该反应的平衡常数表达式为K=$\frac{c({H}_{2})•c({I}_{2})}{{c}^{2}(HI)}$.
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为0.1mol•L-1•min-1
(4)丙容器中:反应开始时V正大于V逆(填“小于”、“等于”或“大于”)
(已知某温度下2HI(g)?H2(g)+I2(g)△H=+AkJ•mol-1 K=4.0)
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol HI | 1mol H2+1mol I2 | 2mol HI+1mol H2+1mol I2 |
| HI的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 吸收akJ | 放出bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
①c1、c3的关系式为2c1=c3
②a、b的关系式为a+b=A
③p2、p3的关系式为2p2=p3
④a1与a2的关系式为α1+α2=1
(2)甲容器中:该反应的平衡常数表达式为K=$\frac{c({H}_{2})•c({I}_{2})}{{c}^{2}(HI)}$.
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为0.1mol•L-1•min-1
(4)丙容器中:反应开始时V正大于V逆(填“小于”、“等于”或“大于”)
16.FeCl3、CuCl2混溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的( )
0 173874 173882 173888 173892 173898 173900 173904 173910 173912 173918 173924 173928 173930 173934 173940 173942 173948 173952 173954 173958 173960 173964 173966 173968 173969 173970 173972 173973 173974 173976 173978 173982 173984 173988 173990 173994 174000 174002 174008 174012 174014 174018 174024 174030 174032 174038 174042 174044 174050 174054 174060 174068 203614
| A. | 加入KSCN的溶液一定不变红色 | B. | 溶液中一定含有Fe3+ | ||
| C. | 溶液中可能含Cu2+ | D. | 剩余固体中一定有铜 |