8.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)Y的元素符号是SS.
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2.
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2.
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
7.NA为阿伏加德罗常数,下列说法错误的是( )
| A. | 0.1 mol的甲基(-CH3)与羟基(-OH)所含电子数均为NA | |
| B. | 1molD216O中含中子、质子、电子各10NA | |
| C. | 32 g S8单质(分子结构如右图)中含有的S-S键个数为NA | |
| D. | 1.5g CH3+中含有的电子数为0.8NA |
6.下列叙述正确的是( )
| A. | 氯化铯晶体中,每1个Cs+与其它8个Cs+等距离紧邻 | |
| B. | 金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子 | |
| C. | 熔点由高到低的顺序是:金刚石>碳化硅>晶体硅 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
5.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式 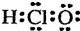 | B. | 钠离子的结构示意图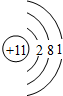 | ||
| C. | 硫原子的最外层电子排布式3s23p4 | D. | 二氧化硅的分子式 SiO2 |
1.某学习小组需0.10mol/L的Na2CO3溶液450mL.下列有关说法正确的是( )
| A. | 称量前应将Na2CO3•xH2O灼烧至恒重 | |
| B. | 配制时需用托盘天平称取4.8 g无水Na2CO3 | |
| C. | 100 mL上述溶液含离子总数为0.03NA | |
| D. | 配制好的Na2CO3溶液应转移到带玻璃塞的试剂瓶中 |
20.通过下列实验现象的分析,对实验事实的解释正确的是( )
0 173654 173662 173668 173672 173678 173680 173684 173690 173692 173698 173704 173708 173710 173714 173720 173722 173728 173732 173734 173738 173740 173744 173746 173748 173749 173750 173752 173753 173754 173756 173758 173762 173764 173768 173770 173774 173780 173782 173788 173792 173794 173798 173804 173810 173812 173818 173822 173824 173830 173834 173840 173848 203614
| A. | 常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸反应 | |
| B. | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性 | |
| C. | H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强 | |
| D. | 向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性 |
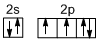 ;
;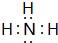 ,B的结构式为
,B的结构式为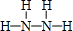 .
. 我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸、密度为1.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸、密度为1.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.