13.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+) ①<②<③ | |
| B. | 在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
12.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L 水中 | |
| B. | 将22.4L氨气溶于水配成1L溶液 | |
| C. | 将1 L10mol•L-1的浓盐酸与9L水混合 | |
| D. | 将4g NaOH溶解在水中配成100mL溶液 |
11.下列实验方案、现象和结论均正确的是( )
| A. |  向里推活塞时,长颈漏斗中有一段水柱,静止,水柱高度不变 该装置的气密性良好 向里推活塞时,长颈漏斗中有一段水柱,静止,水柱高度不变 该装置的气密性良好 | |
| B. |  脱脂棉燃烧 Na2O2与水反应生成氢氧化钠和氧气 脱脂棉燃烧 Na2O2与水反应生成氢氧化钠和氧气 | |
| C. |  烧杯①的澄清石灰水先变浑浊 NaHCO3比Na2CO3受热更易分解 烧杯①的澄清石灰水先变浑浊 NaHCO3比Na2CO3受热更易分解 | |
| D. |  U形管右端的液面高 铁钉发生吸氧腐蚀 U形管右端的液面高 铁钉发生吸氧腐蚀 |
10.把镁带投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度,②镁带的表面积,③溶液的温度,④氯离子的浓度 ⑤滴加硫酸铜溶液.对反应速率有影响的是( )
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③⑤ |
9.下列有关溶液中各类平衡的说法正确的是( )
| A. | 加水稀释0.1mol•L-1 CH3COOH溶液时,溶液中所有离子浓度均减小 | |
| B. | 对FeCl3溶液进行稀释时,Fe3+的水解程度增大,故溶液的酸性增强 | |
| C. | 可根据难溶电解质Ksp的数值大小直接比较难溶电解质在水中的溶解度大小 | |
| D. | 25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl悬浊液中加入KI固体,有黄色沉淀生成 |
7.下列叙述不正确的是( )
| A. | 用熟石灰可处理酸性废水 | B. | 焊锡(锡铅合金)熔点比金属锡高 | ||
| C. | 用丁达尔效应可区分溶液和胶体 | D. | 用热的纯碱溶液可清除油污 |
6.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2SO2(g)+O2?2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)=2CO2 (g)△H1 2C(s)+O2(g)=2CO(g)△H2则△H1<△H2 | |
| D. | 已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3kJ |
5.下列说法错误的是( )
0 173359 173367 173373 173377 173383 173385 173389 173395 173397 173403 173409 173413 173415 173419 173425 173427 173433 173437 173439 173443 173445 173449 173451 173453 173454 173455 173457 173458 173459 173461 173463 173467 173469 173473 173475 173479 173485 173487 173493 173497 173499 173503 173509 173515 173517 173523 173527 173529 173535 173539 173545 173553 203614
| A. | 增大反应物的浓度,可增大活化分子的百分数,从而使反应速率增大 | |
| B. | 决定化学反应速率的主要因素是参加反应的物质的性质 | |
| C. | NH4HCO3 (s)═NH3 (g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| D. | 升温能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的百分数 |
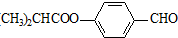 G的一种合成路线如下:
G的一种合成路线如下: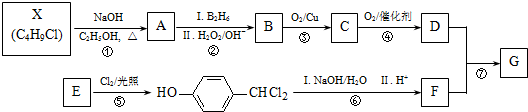
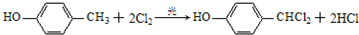 .
. .
. .
.