题目内容
12.下列溶液中物质的量浓度为1mol•L-1的是( )| A. | 将40g NaOH溶解于1L 水中 | |
| B. | 将22.4L氨气溶于水配成1L溶液 | |
| C. | 将1 L10mol•L-1的浓盐酸与9L水混合 | |
| D. | 将4g NaOH溶解在水中配成100mL溶液 |
分析 A、溶液的体积不等于溶剂的体积;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol;
C、由于微粒大小与间隙不同,混合后溶液的体积不等于浓盐酸与水的体积之和;
D、根据n=$\frac{m}{M}$计算氢氧化钠的物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:A、1L水为溶剂的体积,溶液的体积未知,无法计算其浓度,故A错误;
B、HCl所处的状态不确定,22.4LHCl气体的物质的量不一定是1mol,溶于水配成1L溶液,浓度不一定是1mol/L,故B错误;
C、将1 L10mol•L-1的浓盐酸与9L水混合,溶液的体积不等于10L,无法计算其浓度,故C错误;
D、4g NaOH的物质的量为$\frac{4g}{40g/mol}$=0.1mol,溶液体积为100mL,故氢氧化钠溶液的浓度为$\frac{0.1mol}{0.1L}$=1mol/L,故D正确;
故选D.
点评 本题考查物质的量浓度的计算,把握物质的量、质量、体积及浓度的关系为解答该题的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
2.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)═M(g)+N(g),所得实验数据如下表:
请计算:
(1)实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N);
(2)实验②中,该反应的平衡常数K;
(3)实验③中,达到平衡时,X的转化率.
| 实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
(1)实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N);
(2)实验②中,该反应的平衡常数K;
(3)实验③中,达到平衡时,X的转化率.
7.下列叙述不正确的是( )
| A. | 用熟石灰可处理酸性废水 | B. | 焊锡(锡铅合金)熔点比金属锡高 | ||
| C. | 用丁达尔效应可区分溶液和胶体 | D. | 用热的纯碱溶液可清除油污 |
17.体积为1L的某溶液中可能含有Cl-、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$、NH${\;}_{4}^{+}$、Fe3+、Al2+、Ba2+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生的白色沉淀迅速变为灰绿色;过滤、洗涤、灼烧,得到1.6g固体;向上述滤液中加入足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.下列叙述正确的是( )
| A. | 溶液中的主要离子仅为SO${\;}_{3}^{2-}$、Fe2+、NH${\;}_{4}^{+}$ | |
| B. | Cl-一定存在,且c(Cl-)=0.2 mol.L-l | |
| C. | 向原溶液中加入硫酸,可能有气体生成 | |
| D. | CO${\;}_{3}^{2-}$、Al2+一定不存在,K+可能存在 |
4.某温度下 H2(g)+I2(g)?2HI(g)的平衡常数K=O.25,该温度下在甲、乙、丙三个恒容密闭容器中充入H2(g)、I2(g),起始浓度如下表所示:
下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2/mol•L-1 | 0.010 | 0.020 | 0.020 |
| c(I2)/mol•L-1 | 0.010 | 0.010 | 0.020 |
| A. | 平衡时甲中和丙中H2的转化率相同 | |
| B. | 平衡时乙中I2的转化率小于40% | |
| C. | 平衡时乙中c(HI)比甲中的2倍大 | |
| D. | 反应平衡时,丙中气体颜色最深,乙中气体颜色最浅 |
1.你认为下列说法不合理的是( )
| A. | 塑料制品长期不使用也会老化 | |
| B. | 可以通过与盐酸的互滴实验鉴别碳酸钠和碳酸氢钠 | |
| C. | 过氧化钠可以作供氧剂,可以和二氧化硫反应生成亚硫酸钠和氧气 | |
| D. | 纯碱是 Na2C03,小苏打是 NaHC03,其水溶液均呈碱性 |
2.图象能直观地反映有关物理量的变化及规律,下列各图象与描述相符的是( )
 A.如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 A.如图表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 | 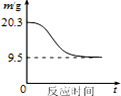 B.如图表示 0.1mol MgCl2•6H2O在空气中充分加热时固体质量随时间的变化 B.如图表示 0.1mol MgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | 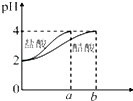 C.如图表示分别稀释10mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100 C.如图表示分别稀释10mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100 | 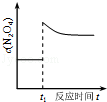 D.如图表示平衡2NO2(g)?N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 D.如图表示平衡2NO2(g)?N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
| A. | A | B. | B | C. | C | D. | D |



