1.在一定条件下,将1molCO和1mol水蒸气通入容器中发生下述反应:CO+H2O═CO2+H2,达到平衡后,测得为CO20.6mol,再通入0.3mol水蒸气,又达到平衡后,CO2的物质的量为( )
| A. | 0.7mol | B. | 0.8mol | C. | 0.6mol | D. | 0.9mol |
20.高效水处理剂ClO2在实验室中通过以下反应制得:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法不正确的是( )
| A. | CO2 是氧化产物 | |
| B. | 1mol KClO3 参加反应,转移的电子为1mol | |
| C. | KClO3 在反应中被氧化 | |
| D. | H2C2O4的还原性强于ClO2 的还原性 |
19.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性无色溶液中:K+、Fe3+、Cl-、SO42- | |
| B. | 滴加石蕊试液显红色的溶液:K+、Mg2+、Cl-、NO3- | |
| C. | 含有0.1mol•L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 滴加酚酞试液显红色的溶液:Ba2+、H+、NO3-、Cl- |
18.现有7瓶失去了标签的液体,可能是:①乙醇,②乙酸,③苯,④乙酸乙酯,⑤油脂,⑥葡萄糖溶液,⑦蔗糖溶液.现通过如表实验步骤来确定各试剂瓶中所装的液体名称.
试给它们的试剂瓶重新贴上标签:
B乙酸,D乙酸乙酯,E油脂,F葡萄糖,G蔗糖溶液.
| 实验步骤和方法 | 实验现象 |
| 1.把7瓶液体分别依次标号A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| 2.各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
| 3.分别取少量7种液体于试管中加新制的Cu(OH)2悬浊液并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
| 4.各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且E中发生了皂化反应 |
B乙酸,D乙酸乙酯,E油脂,F葡萄糖,G蔗糖溶液.
17.已知,T℃温度下,反应:N2(g)+3H2(g)?2NH3(g)△H<0的平衡常数K=9.向容积固定的某真空容器中充入N2(g)、H2(g)和NH3(g),使其浓度分别为3mol/L、1mol/L和50mol/L,在T℃温度下发生上述反应.下列说法中正确的是( )
| A. | 反应开始后,反应要放出能量 | |
| B. | 建立平衡状态时c(N2)<3 mol/L | |
| C. | 该条件下,平衡时N2的体积分数为$\frac{1}{14}$ | |
| D. | 反应条件变化时,其K值也一定发生变化 |
13.甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸气重整.向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
回答下列问题:
(1)反应CO(g)+H2O(g)═CO2(g)+H2(g)的△H=-41.2kJ•mol-1.
(2)在初始阶段,甲烷蒸气重整的反应速率小于甲烷氧化的反应速率(填“大于”、“小于”或“等于”).
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)的Kp=$\frac{{p}^{3}({H}_{2})×p(CO)}{p(C{H}_{4})×p({H}_{2}O)}$; 随着温度的升高,该平衡常数增大(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于放热的甲烷氧化反应为吸热的蒸气重整提供能量.
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
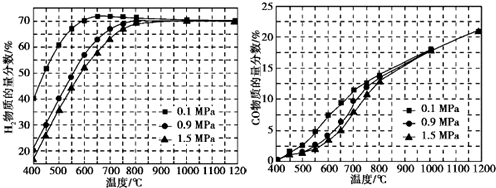
①若要达到H2物质的量分数>65%、CO物质的量分数<10%,以下条件中最合适的是B.
A.600℃,0.9MPa B.700℃,0.9Mpa
C.800℃,1.5MPa D.1 000℃,1.5MPa
②画出600℃,0.1MPa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是导致生成的氢气和氧气反应.
| 反应过程 | 化学方程式 | 焓变△H(kJ/mol) | 活化能Ea(kJ/mol) |
| 甲烷氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
(1)反应CO(g)+H2O(g)═CO2(g)+H2(g)的△H=-41.2kJ•mol-1.
(2)在初始阶段,甲烷蒸气重整的反应速率小于甲烷氧化的反应速率(填“大于”、“小于”或“等于”).
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp),则反应CH4(g)+H2O(g)?CO(g)+3H2(g)的Kp=$\frac{{p}^{3}({H}_{2})×p(CO)}{p(C{H}_{4})×p({H}_{2}O)}$; 随着温度的升高,该平衡常数增大(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于放热的甲烷氧化反应为吸热的蒸气重整提供能量.
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:

①若要达到H2物质的量分数>65%、CO物质的量分数<10%,以下条件中最合适的是B.
A.600℃,0.9MPa B.700℃,0.9Mpa
C.800℃,1.5MPa D.1 000℃,1.5MPa
②画出600℃,0.1MPa条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:

(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是导致生成的氢气和氧气反应.
12.下列依据热化学方程式得出的结论正确的是( )
0 173323 173331 173337 173341 173347 173349 173353 173359 173361 173367 173373 173377 173379 173383 173389 173391 173397 173401 173403 173407 173409 173413 173415 173417 173418 173419 173421 173422 173423 173425 173427 173431 173433 173437 173439 173443 173449 173451 173457 173461 173463 173467 173473 173479 173481 173487 173491 173493 173499 173503 173509 173517 203614
| A. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0gNaOH的稀溶液与足量稀醋酸完全中和,放出的热量小于57.3kJ | |
| B. | 2C(s)+2O2(g)═2CO2(g)△H=akJ•mol-1:2C(s)+O2(g)═2CO(g)△H=bkJ•mol-1,则a>b | |
| C. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g);△H=+285.5 kJ•mol-1 | |
| D. | 已知正丁烷(g)→异丁烷(g)△H<0,则正丁烷比异丁烷稳定 |
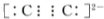
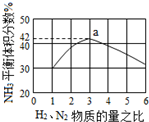 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,氨是最重要的氮肥,是产量最大的化工产品之一.其工业合成原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在密闭容器中,使2mol N2和6mol H2混合发生以上反应.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,氨是最重要的氮肥,是产量最大的化工产品之一.其工业合成原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在密闭容器中,使2mol N2和6mol H2混合发生以上反应.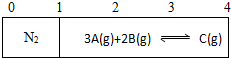 一刚性容器内部有一个不漏气且可滑动的活塞将容器分成左右两个室,左室内充入一定体积的N2气体,右室充入A和B两种气体,且A和B的物质的量之比为3:2,右室内发生如下反应:3A(g)+2B(g)?C(g).反应开始前活塞停留在离左端1/4处(如图),反应在恒温下进行,当反应达平衡状态时,活塞处于容器中间.
一刚性容器内部有一个不漏气且可滑动的活塞将容器分成左右两个室,左室内充入一定体积的N2气体,右室充入A和B两种气体,且A和B的物质的量之比为3:2,右室内发生如下反应:3A(g)+2B(g)?C(g).反应开始前活塞停留在离左端1/4处(如图),反应在恒温下进行,当反应达平衡状态时,活塞处于容器中间.