8.当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A. | 淀粉溶液 | B. | 泥水 | C. | NaCl 溶液 | D. | 浓盐酸 |
6.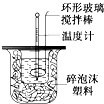 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:
①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度. 回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1.
(2)倒入NaOH溶液的正确操作是:C. (从下列选项中选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入C.一次迅速倒入
(3)实验数据如下表:
①请填写下表中的空白:
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8kJ/mol ( 取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)a、b、c.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度. 回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1.
(2)倒入NaOH溶液的正确操作是:C. (从下列选项中选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入C.一次迅速倒入
(3)实验数据如下表:
①请填写下表中的空白:
| 温度 实验 次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)a、b、c.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
5.工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图1:
(1)此流程的第II步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
从上表可以推断:此反应是放(填“吸”或“放”)热反应.在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为66.7%.
(2)在500℃,按照下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是AD.
A.2c1=c2=c3 B.2Q1=Q2=Q3 C.α1=α2=α3 D.α1+α2=1
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是②③.
①v(CO2)正=v(H2O)逆 ②混合气体的密度不变
③混合气体的平均相对分子质量不变④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化
(4)如图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件使浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸气的量(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).

(1)此流程的第II步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,按照下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是AD.
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是②③.
①v(CO2)正=v(H2O)逆 ②混合气体的密度不变
③混合气体的平均相对分子质量不变④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化
(4)如图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件使浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸气的量(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).

4.硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH-═O2NC6H4COO-+C2H5OH,两种反应物的初始浓度均为0.050mol•L-1,15℃时测得O2NC6H4COOC2H5的浓度c随时间变化的数据如表所示.回答下列问题:
(1)计算该反应在120~180s间的平均反应速率7.3×10-5mol/(L•s);比较120~180s与180~240s 区间的平均反应速率的大小,前者>后者(填>,<或=),理由是随着反应进行,反应物浓度降低,反应速率减慢.
(2)计算15℃时该反应的平衡常数5.4.
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有BC.
A.加入O2NC6H4COOC2H5
B.增加OH-的浓度
C.移去产物
D.加入适当的催化剂.
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| c/mol•L-1 | 0 | 0.036 | 0.030 | 0.026 | 0.022 | 0.017 | 0.016 | 0.015 | 0.015 |
(2)计算15℃时该反应的平衡常数5.4.
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有BC.
A.加入O2NC6H4COOC2H5
B.增加OH-的浓度
C.移去产物
D.加入适当的催化剂.
3. (1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:
(1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:
请回答下列问题:
①如图表示某反应的能量变化关系图,此反应为放热(填“放热”或“吸热”)反应,其中△H=C-DkJ•mol-1(用含C和D的字母表示).
②若此能量变化关系图表示反应H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则B=926kJ•mol-1,x=496.4
(2)①火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.已知:
N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g),△H=-98kJ•mol-1
H2O(l)═H2O(g),△H=+44kJ•mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642kJ•mol-1.
②肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.该电池放电时,负极的电极反应式是N2H4+4OH--4e-=4H2O+N2.
 (1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:
(1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:| 化学键 | H-H | O═O | O-H |
| 键能 (kJ•mol-1) | 436 | x | 463 |
①如图表示某反应的能量变化关系图,此反应为放热(填“放热”或“吸热”)反应,其中△H=C-DkJ•mol-1(用含C和D的字母表示).
②若此能量变化关系图表示反应H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则B=926kJ•mol-1,x=496.4
(2)①火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.已知:
N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g),△H=-98kJ•mol-1
H2O(l)═H2O(g),△H=+44kJ•mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642kJ•mol-1.
②肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.该电池放电时,负极的电极反应式是N2H4+4OH--4e-=4H2O+N2.
2.乙苯催化脱氢制苯乙烯反应: 已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
 已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.| A. | -124 | B. | +124 | C. | -288 | D. | +288 |
1.将BaO2放入密闭的真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡.保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| A. | 平衡常数减小 | B. | BaO量不变 | C. | 氧气浓度不变 | D. | 平衡向右移动 |
20.下列事实不能用勒沙特列原理解释的是( )
| A. | 氯化镁溶液加热蒸干最终得不到氯化镁固体 | |
| B. | 实验室可用排饱和食盐水的方法收集氯气 | |
| C. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| D. | 压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
19.在进行中和反应的反应热测定的实验中不需要用到的仪器是( )
0 173174 173182 173188 173192 173198 173200 173204 173210 173212 173218 173224 173228 173230 173234 173240 173242 173248 173252 173254 173258 173260 173264 173266 173268 173269 173270 173272 173273 173274 173276 173278 173282 173284 173288 173290 173294 173300 173302 173308 173312 173314 173318 173324 173330 173332 173338 173342 173344 173350 173354 173360 173368 203614
| A. | 天平 | B. | 温度计 | C. | 环形玻璃搅拌棒 | D. | 量筒 |
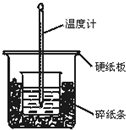 通过测定反应过程中所放出的热量可计算中和热.50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在图示的装置中进行中和反应.回答下列问题:
通过测定反应过程中所放出的热量可计算中和热.50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在图示的装置中进行中和反应.回答下列问题: