题目内容
3. (1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:
(1)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些化学键的键能:| 化学键 | H-H | O═O | O-H |
| 键能 (kJ•mol-1) | 436 | x | 463 |
①如图表示某反应的能量变化关系图,此反应为放热(填“放热”或“吸热”)反应,其中△H=C-DkJ•mol-1(用含C和D的字母表示).
②若此能量变化关系图表示反应H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则B=926kJ•mol-1,x=496.4
(2)①火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.已知:
N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g),△H=-98kJ•mol-1
H2O(l)═H2O(g),△H=+44kJ•mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642kJ•mol-1.
②肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.该电池放电时,负极的电极反应式是N2H4+4OH--4e-=4H2O+N2.
分析 (1)①从反应物和生成物能量大小分析;△H=-(反应物总能量-生成物总能量);
②△H=反应物键能和-生成物键能和,键能和等于其活化能;
(2)①根据盖斯定律,将所给的反应通过加减乘除得到所要求的目标反应,反应热做相应的变化即可;
②肼-空气燃料电池放电时,负极上肼失电子和氢氧根离子反应生成H2O和氮气,正极上氧气得电子和水反应生成氢氧根离子,据此分析解答.
解答 解:(1)①反应物能量高于生成物,正反应放热;△H=-(反应物总能量-生成物总能量)=-(D-C)KJ/mol=(C-D)KJ/mol,
故答案为:放热;(C-D);
②B表示1mol水的键能,为2×463KJ/mol=926KJ/mol;△H=反应物键能和-生成物键能和=436KJ/mol+$\frac{1}{2}$xKJ/mol-2×463KJ/mol=-241.8KJ/mol,x=496.4KJ/mol,
故答案为:926;496.4;
(2)①N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1①
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g),△H=-98kJ•mol-1②
H2O(l)═H2O(g),△H=+44kJ•mol-1③
将①+2②+4③可得:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=(-534kJ•mol-1)+2×(-98kJ•mol-1)+4×(+44kJ•mol-1)=-642 kJ•mol-1
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642 kJ•mol-1;
②肼-空气燃料电池放电时,负极上肼失电子和氢氧根离子反应生成H2O和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:N2H4+4OH--4e-=4H2O+N2.
点评 本题考查电极反应式的书写、盖斯定律的运用,明确各个电极上发生的反应是解本题关键,注意要结合电解质溶液酸碱性书写电极反应式,为考查重点.

| A. | AB | B. | AB2 | C. | AB3 | D. | A2B |
| A. | 升高温度,活化分子百分数增加,化学反应速率一定增大 | |
| B. | 增大压强,可使活化分子百分数增多,化学反应速率一定增大 | |
| C. | 加入反应物可使活化分子百分数大大增加,化学反应速率大大加快 | |
| D. | 活化分子间所发生的碰撞均为有效碰撞 |
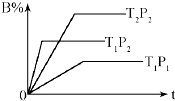 已知某可逆反应 mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确是( )
已知某可逆反应 mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确是( )| A. | T2>T1?P1>P2 m+n>p??△Η<0 | B. | T1>T2?P1<P2 m+n<p??△Η>0 | ||
| C. | T1<T2?P1<P2 m+n<p??△Η<0 | D. | T1>T2?P1<P2 m+n>p??△Η>0 |
| A. | 淀粉溶液 | B. | 泥水 | C. | NaCl 溶液 | D. | 浓盐酸 |
| A. | 金属冶炼 | B. | 燃放鞭炮 | C. | 食物腐败 | D. | 煅烧石灰石 |
| A. | 取少量晶体放入试管中,加热,若试管口上蘸有少量无水硫酸铜粉末的脱脂棉变蓝,则可证明晶体中含有结晶水 | |
| B. | 取少量晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量晶体放入试管,加入少量稀NaOH溶液,在试管口用湿润的蓝色石蕊试纸检验,若变红,则可证明晶体的成分中含有NH4+ | |
| D. | 取少量晶体溶于水,加适量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
 的名称为3,3,4-三甲基己烷
的名称为3,3,4-三甲基己烷 的名称为3-甲基-1-戊烯
的名称为3-甲基-1-戊烯
 .
.