14.下列叙述不正确的是( )
| A. | 常温常压下,3.2gO2所含的原子数为0.2NA | |
| B. | 标准状况下,18gH2O所含的氧原子数目为NA | |
| C. | 常温常压下,92gNO2和N2O4的混合气体中含有的原子总数为6NA | |
| D. | 标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA |
13.检验某未知溶液中是否含有SO${\;}_{4}^{2-}$的下列操作中最合理的是( )
| A. | 加入硝酸酸化的Ba(NO3)2 | B. | 先加HNO3酸化,再加Ba(NO3)2溶液 | ||
| C. | 先加盐酸酸化,再加BaCl2溶液 | D. | 加入盐酸酸化了的BaCl2溶液 |
11.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol 苯乙烯中含有的碳碳双键数为4NA | |
| B. | 25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA | |
| C. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| D. | 足量的Fe和1mol Cl2完全反应,转移的电子数为3NA |
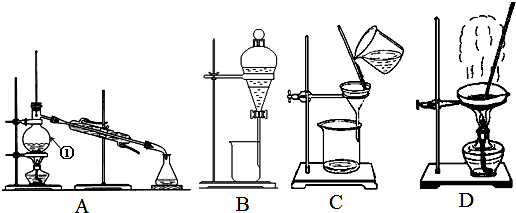
10.利用右图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
9.以下物质在水溶液中的电离方程式错误的是( )
| A. | MgSO4═Mg2++SO42- | B. | Fe(OH)3═Fe3++3OH- | ||
| C. | NaHCO3═Na++HCO3- | D. | KAl(SO4)2═K++Al3++2SO42- |
7.硅元素有质量数为28、29、30三种同位素,硅元素的近似相对原子质量为28.1,自然界中质量数为28的硅原子百分含量为92%,则质量分数为29、30的原子个数比为( )
| A. | 3:5 | B. | 3:1 | C. | 2:3 | D. | 3:2 |
6.完全中和10.2g二元酸H2A生成正盐,用去24g NaOH,则有关此二元酸的下列说法正确是( )
0 172694 172702 172708 172712 172718 172720 172724 172730 172732 172738 172744 172748 172750 172754 172760 172762 172768 172772 172774 172778 172780 172784 172786 172788 172789 172790 172792 172793 172794 172796 172798 172802 172804 172808 172810 172814 172820 172822 172828 172832 172834 172838 172844 172850 172852 172858 172862 172864 172870 172874 172880 172888 203614
| A. | 该酸的摩尔质量为34 | B. | 该酸的分子量为17 | ||
| C. | 10.2g该酸的物质的量是0.3mol | D. | 该酸一定是强酸 |

 爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。
爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。