15.各组性质比较的表示中,正确的是( )
| A. | 沸点:Cl2<2<Br2<I2 | B. | 沸点:HF<HCl<HBr<HI | ||
| C. | 氧化性:F2<Cl2<Br2<I2 | D. | 还原性:HF<HCl<HBr<HI |
12. 在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
 在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )
在某密闭容器中,可逆反应:A(g)+B(g)?C(g)符合图中(Ⅰ)所示关系,φ(C)表示C气体在混合气体中的体积分数.由此判断,对图象(Ⅱ)说法不正确的是( )| A. | p3>p4,Y轴表示A的转化率 | |
| B. | p3>p4,Y轴表示B的质量分数 | |
| C. | p3>p4,Y轴表示B的转化率 | |
| D. | p3>p4,Y轴表示混合气体的平均相对分子质量 |
11.下列溶液中导电性最强的是( )
| A. | 1 L 0.1 mol/L醋酸 | B. | 0.1 L 0.1 mol/L H3PO4溶液 | ||
| C. | 0.5 L 0.1 mol/L盐酸 | D. | 2 L 0.1 mol/L H2SO3溶液 |
10.亚硝酸溶液中离子和分子同时存在则亚硝酸是( )
| A. | 弱电解质 | B. | 强电解质 | C. | 非电解质 | D. | 混合物 |
9.密闭容器中进行如下反应:X2(g)+3Y2(g)?2Z(g),X2、Y2、Z的起始浓度分别为0.2mol/L、0.6mol/L,0.4mol/L当达到平衡时,下列数据肯定正确的是( )
| A. | X2为0.4 mol/L,Y2为1.2 mol/L | B. | Y2为1.6 mol/L | ||
| C. | X2为0.3 mol/L,Z为0.2 mol/L | D. | Z为1.0 mol/L |
8.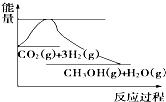 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )| A. | △H<0,△S<0 | B. | △H>0,△S<0 | C. | △H>0,△S>0 | D. | △H<0,△S>0 |
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 用排饱和食盐水法收集Cl2 | |
| B. | 冰镇的啤酒打开后泛起泡沫 | |
| C. | 加压有利于合成氨反应 | |
| D. | 金属铝、铁与同浓度的盐酸反应铝的速度快 |
6.在一定条件下,反应:2NO+O2?2ΝΟ2在定容容器中发生,对该反应达到平衡的标志的描述中,错误的是( )
①混合气体的总分子数不再变化
②混合气体的颜色不再变化
③容器的总压强不再变化
④混合气体的总质量不再变化
⑤混合气体的密度不再变化
⑥单位时间内生成nmol的NO,同时消耗nmol的NO2.
0 172684 172692 172698 172702 172708 172710 172714 172720 172722 172728 172734 172738 172740 172744 172750 172752 172758 172762 172764 172768 172770 172774 172776 172778 172779 172780 172782 172783 172784 172786 172788 172792 172794 172798 172800 172804 172810 172812 172818 172822 172824 172828 172834 172840 172842 172848 172852 172854 172860 172864 172870 172878 203614
①混合气体的总分子数不再变化
②混合气体的颜色不再变化
③容器的总压强不再变化
④混合气体的总质量不再变化
⑤混合气体的密度不再变化
⑥单位时间内生成nmol的NO,同时消耗nmol的NO2.
| A. | ①②③ | B. | ④⑤⑥ | C. | ①②④ | D. | ③⑤⑥ |
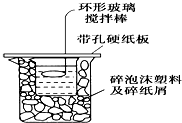 50mL 0.50mol/L的盐酸和50mL 0.55mol/L的烧碱溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,试回答下列问题:
50mL 0.50mol/L的盐酸和50mL 0.55mol/L的烧碱溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,试回答下列问题: