16.某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4•5H2O,实现废物综合利用,实验过程如下:
过程Ⅰ:
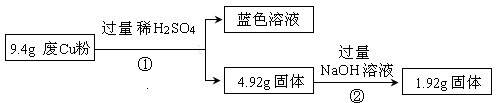
(1)废Cu粉中一定含有的杂质是Fe2O3、SiO2(填化学式)
(2)写出过程②发生反应的离子方程式:SiO2+2OH-═SiO32-+H2O.
过程Ⅱ:
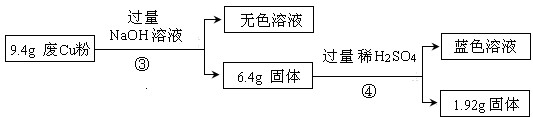
(3)综合过程Ⅰ、II,计算废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(化为最简整数比)
过程Ⅲ:已知25℃时:
(4)在Ⅱ中所得蓝色溶液中加入一定量的H2O2 溶液,调节溶液的pH范围为4.0≤pH<5.4,然后过滤、结晶,可得CuSO4•5H2O.
(5)下列与Ⅲ方案 相关的叙述中,正确的是ACD填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在.
过程Ⅰ:

(1)废Cu粉中一定含有的杂质是Fe2O3、SiO2(填化学式)
(2)写出过程②发生反应的离子方程式:SiO2+2OH-═SiO32-+H2O.
过程Ⅱ:

(3)综合过程Ⅰ、II,计算废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(化为最简整数比)
过程Ⅲ:已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(5)下列与Ⅲ方案 相关的叙述中,正确的是ACD填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在.
14.Al、Fe、Cu都是重要而常见的金属,下列有关说法正确的是( )
| A. | 三者的单质在常温下都能溶于浓硫酸和浓硝酸 | |
| B. | 三者的单质放置在空气中均只生成氧化物 | |
| C. | 三者所对应的氢氧化物在水中都存在溶解平衡 | |
| D. | 工业上制备这三种金属的方法依次为电解法、热分解法和热还原法 |
13.下列关于Cl、N、S等非金属元素单质及其化合物的说法正确的是( )
| A. | 漂白粉的成分是次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥硫化氢 | |
| C. | 将浓氨水滴到氢氧化钠固体中可以制取氨气 | |
| D. | 单质氯气及单质硫与铁反应生成的产物中,铁的化合价相同 |
7.反应A+3B=2C+2D在不同条件下反应速率如下,其中最快的是反应( )
0 172634 172642 172648 172652 172658 172660 172664 172670 172672 172678 172684 172688 172690 172694 172700 172702 172708 172712 172714 172718 172720 172724 172726 172728 172729 172730 172732 172733 172734 172736 172738 172742 172744 172748 172750 172754 172760 172762 172768 172772 172774 172778 172784 172790 172792 172798 172802 172804 172810 172814 172820 172828 203614
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) | |
| C. | v(C)=0.4mol/(L•min) | D. | v(D)=0.0075 mol/(L•s) |
| A. | A | B. | B | C. | C | D. | D |
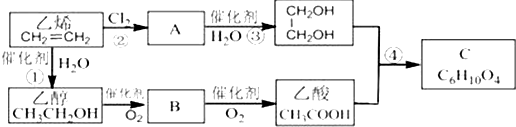
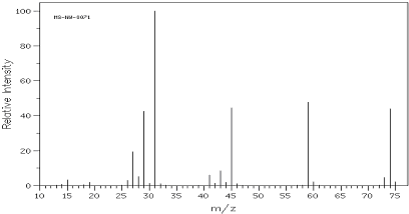

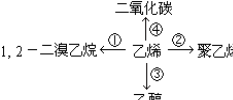
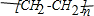 ③CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH④CH2=CH2+3O2$\stackrel{点燃}{→}$2CO2+2H2O.
③CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH④CH2=CH2+3O2$\stackrel{点燃}{→}$2CO2+2H2O.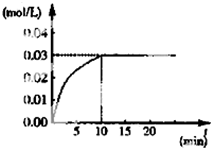 在某一容积为5L的体积不变的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的体积不变的密闭容器内,加入 0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图: 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.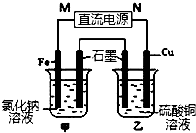 如图装置中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5mol/L的CuSO4溶液.向甲烧杯中滴入几滴酚酞,反应一段时间后,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为变小(选填“变大”、“变小”、“不变”).通电一段时间后(溶液中还有CuSO4),停止通电.若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).
如图装置中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5mol/L的CuSO4溶液.向甲烧杯中滴入几滴酚酞,反应一段时间后,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为变小(选填“变大”、“变小”、“不变”).通电一段时间后(溶液中还有CuSO4),停止通电.若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).