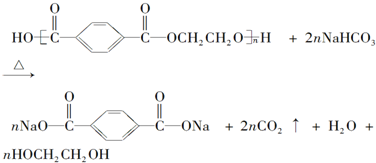
2.已知下列数据:
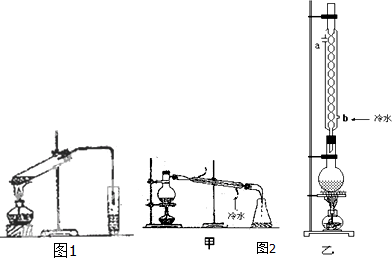
实验室制乙酸乙酯的主要装置如图1所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到15mL试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处,③小火加热试管中的混合液;④待小试管中收集约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯.
请同学们回答下列问题:
(1)写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,浓H2SO4的作用是催化剂、吸水剂.
(2)步骤④所观察到的现象是在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,原因是上层是油层因为生成的乙酸乙酯难溶于水,且密度比水小,同时因为挥发出来的乙酸与碳酸钠反应,放出CO2气体,所以有气泡出现.
(3)步骤⑤中,分离出乙酸乙酯选用的仪器是分液漏斗.
(4)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如图2甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物).你认为哪种装置合理,为什么?答:乙,反应物能冷凝回流.
| 物 质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 乙 醇 | -114 | 78 | 0.789 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |

实验室制乙酸乙酯的主要装置如图1所示,主要步骤为:①在30mL的大试管中按体积比1:4:4的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到15mL试管所盛饱和Na2CO3溶液(加入1滴酚酞试液)上方2mm~3mm处,③小火加热试管中的混合液;④待小试管中收集约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层;⑤分离出纯净的乙酸乙酯.
请同学们回答下列问题:
(1)写出该反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,浓H2SO4的作用是催化剂、吸水剂.
(2)步骤④所观察到的现象是在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,原因是上层是油层因为生成的乙酸乙酯难溶于水,且密度比水小,同时因为挥发出来的乙酸与碳酸钠反应,放出CO2气体,所以有气泡出现.
(3)步骤⑤中,分离出乙酸乙酯选用的仪器是分液漏斗.
(4)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如图2甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取烧瓶中产物).你认为哪种装置合理,为什么?答:乙,反应物能冷凝回流.
1.有关金属钠的叙述正确的是 ( )
| A. | 钠的密度比煤油大,保存在煤油中 | |
| B. | 金属钠质软,可以用小刀切割 | |
| C. | 钠的熔点比水大,钠投入到水中放热反应生成的气体中有大量水蒸气 | |
| D. | Na比Cu活泼,因而可以从Cu的盐溶液中置换出铜 |
20.下列说法不正确的是( )
| A. | 4.5g SiO2晶体中含有的硅氧键的数目为0.3NA | |
| B. | 向FeI2溶液中通入适量C12,当有1mol1Fe2+被氧化时,共转移的电子的数目为3NA | |
| C. | 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA | |
| D. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
19.制备FeSO4最适宜的方法是( )
| A. | 过量的铁与稀H2SO4反应 | B. | FeO与H2SO4反应 | ||
| C. | FeCO3与H2SO4稀反应 | D. | Fe(OH)3与稀H2SO4反应 |
18.下列各组离子在水溶液里能大量共存.但用盐酸酸化后却不能大量共存的离子组是( )
| A. | Mg+、Al3+、Cl-、NO3- | B. | Fe2+、Na+、NO3-、SO42- | ||
| C. | Ba2+、Na+、K+、NO3- | D. | K+、Ca2+、CO32-、OH- |
17.m g铜、铁的混合物与一定量浓硝酸完全反应后,向所得到的溶液中滴加KSCN,溶液变为血红色,将所得气体与3.36L O2(标准状况)混合后通入水中,所有气体能完全被水吸收生成硝酸.若向所得溶液中加入NaOH溶液至恰好完全沉淀,则生成沉淀的质量为( )
| A. | (m+4.8)g | B. | (m+5.1)g | C. | (m+10.2)g | D. | (m+19.2)g |
16.下列反应中,下面划线的元素被氧化的是( )
0 172434 172442 172448 172452 172458 172460 172464 172470 172472 172478 172484 172488 172490 172494 172500 172502 172508 172512 172514 172518 172520 172524 172526 172528 172529 172530 172532 172533 172534 172536 172538 172542 172544 172548 172550 172554 172560 172562 172568 172572 172574 172578 172584 172590 172592 172598 172602 172604 172610 172614 172620 172628 203614
| A. | Cl2+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2 | |
| B. | SO2+2H2S═3S↓+2H2O | |
| C. | 8CuFeS2+21O2$\frac{\underline{\;高温\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2 | |
| D. | NH3+HNO3═NH4NO3 |