8.下列有关化学现象及反应事实的解释中,方程式书写正确的是( )
| A. | 氢硫酸显弱酸性:H2S?2H++S2- | |
| B. | Na2CO3水溶液显弱碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 用铜电极电解饱和NaCl溶液:阳极反应式是:2Cl--2e-=Cl2↑ | |
| D. | 用稀硝酸洗去试管中的银镜:3Ag+NO3-+4H+=3Ag++NO↑+2H2O |
7.某无色溶液中可能含有I-、NH4+、Cu2+、SO32-中的若干种,向溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液的组成的判断正确的是( )
①肯定含I- ②肯定含SO32- ③肯定含NH4+ ④可能含I- ⑤一定不含Cu2+.
①肯定含I- ②肯定含SO32- ③肯定含NH4+ ④可能含I- ⑤一定不含Cu2+.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ②③④⑤ |
6.NA为阿伏加德罗常数的值,下列说法中错误的是( )
| A. | 12g金刚中含共价键数目为2NA | |
| B. | 密闭容器中2molNO与1molO2充分反应,生成物的分子数为2NA | |
| C. | 常温下,10L,PH=13的Ba(OH)2溶液含OH-的数目为NA | |
| D. | 过氧化钠与水反应时,生成1molO2时转移电子数为2NA |
5.下列各反应中,生成物不随反应条件或反应物用量的变化而变化的是( )
| A. | Na和O2 | B. | Fe和稀HNO3 | C. | Cu和FeCl3溶液 | D. | Na2CO3和稀HCl |
3.某温度下水的离子积常数 Kw=1.0×10-12.在此温度下,已知某强酸溶液pH=a,某强碱溶液的pH=b,已知a+b=13,酸碱溶液混合后恰好完全反应,则酸溶液的体积V(酸)和碱溶液的体积V(碱)的正确关系是( )
| A. | V(碱)=10V(酸) | B. | V(酸)=10V(碱) | C. | V(酸)=2V(碱) | D. | V(酸)=V(碱) |
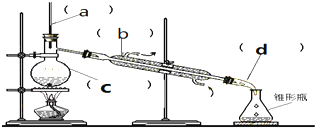
2.如图所示是分离混合物时常用的仪器,从左至右,说法错误的是( )
0 172373 172381 172387 172391 172397 172399 172403 172409 172411 172417 172423 172427 172429 172433 172439 172441 172447 172451 172453 172457 172459 172463 172465 172467 172468 172469 172471 172472 172473 172475 172477 172481 172483 172487 172489 172493 172499 172501 172507 172511 172513 172517 172523 172529 172531 172537 172541 172543 172549 172553 172559 172567 203614

| A. | 仪器C是圆底烧瓶,加热时,液体量不超过容积的$\frac{2}{3}$,不少于容积的$\frac{1}{3}$ | |
| B. | 仪器b是直型冷凝管 | |
| C. | 仪器b中冷却水的进出方向是“下进上出” | |
| D. | 进行蒸馏操作时,温度计的下端不能放在液面以下 |



 +H2O$→_{△}^{稀H_{2}SO_{4}}$
+H2O$→_{△}^{稀H_{2}SO_{4}}$ +CH3OH③F→G:2
+CH3OH③F→G:2 等
等
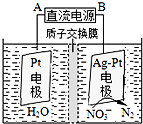 为治理环境,减少雾霾,工业上通常用下列方法治理CO2和硫、氮氧化物的污染.
为治理环境,减少雾霾,工业上通常用下列方法治理CO2和硫、氮氧化物的污染.